Перенос - углеводород
Cтраница 1
Диффузионно-фильтрационный перенос углеводородов к поверхности в присутствии природных катализаторов сопровождается разрывом длинных цепей углеводородов на более мелкие молекулы, что приводит к насыщению покрышки свободными электронами. Поэтому зона, простирающаяся от резервуара вверх ( 10 - 150м), и сам резервуар насыщаются отрицательными зарядами и являются, соответственно, зонами восстановления. [1]
Изменения свободной энергии в процессе переноса углеводородов из воды в водные растворы имеют отрицательные значения и уменьшаются с повышением температуры, что является характерной особенностью ГВ. [2]
Изменения свободной анергии в процессе переноса углеводородов из воды в водные растворы имеют отрицательные значения и уменьшаются с повышением температуры, что является характерной особенностью ЕВ. [3]
Установленный характер изменения термодинамических функций процесса переноса углеводородов из воды в водные растворы аммиака, диэтиламина и солей тетраалкиламмония в зависимости от концентрации всаливателя и температуры также может быть объяснен с точки зрения гидрофобного взаимодействия между молекулами углеводорода и всаливателя. [4]
Температурная зависимость изменения энтальпии и энтропии переноса углеводородов хорошо соответствует рассчитанной Веном и Хан-гом [6] термодинамике процесса растворения насыщенных углеводородов GI - С4 в водных растворах бромидов тетраалкиламмония. [5]
Установленный характер изменения термодинамических функций процесса переноса углеводородов из воды в водные растворы аммиака, диэтиламина и солей тетраалкиламмония в зависимости от концентрации всаливателя и температуры также может быть объяснен с точки зрения гидрофобного взаимодействия между молекулами углеводорода и всаливателя. [6]
Температурная зависимость изменения энтальпии и энтропии переноса углеводородов хорошо соответствует рассчитанной Веном и Хан-гом [6] термодинамике процесса растворения насыщенных углеводородов d - 4 в водных растворах бромидов тетраалкиламмония. Если для тетрабутиламмонийбромида, а также диэтиламина и аммиака характерно увеличение А / / и AS n с ростом температуры, то в случае солей тетраметил - и тетраэтиламмония имеет место некоторое уменьшение положительных изменений энтальпии и энтропии процесса переноса. [7]
Показана роль сжатых газов в извлечении и переносе углеводородов, а также в образовании нефтяных, газовых и некоторых рудных месторождений. Освещаются вопросы применения сжатых газов для разделения смесей термически неустойчивых веществ и для экстракции. Приводятся материалы по использованию сжатых газов для увеличения нефтеотдачи пласта. [8]
Какие природные газы могут принимать участие в переносе углеводородов из материнских пород в коллекторы осадочных пород. Это газы, которые образуются при преобразовании рассеянного и концентрированного ( угли) ОВ, находящегося в осадочных породах, а также газы, поднимающиеся из глубин по разломам. Рассмотрим первый источник с количественной стороны. [9]
Таким образом, расчет основных термодинамических функций процессов переноса углеводородов из воды в водные растворы аммиака, диэтиламина и тетраалкиламмониевых солей подтверждает вывод о том, что одной из главных причин повышения растворимости углеводородов в изученных водных растворах является гидрофобное взаимодействие между молекулами углеводорода и всаливателя. [10]
Таким образом, расчет основных термодинамических функций процессов переноса углеводородов из воды в водные растворы аммиака, дизтиламина и тетраалкиламмониевых солей подтверждает вывод о том, что одной из главных причин повышения растворимости углеводородов в изученных водных растворах является гидрофобное взаимодействие между молекулами углеводорода и всэливателя. [11]
С повышением температуры ба и Дба уменьшаются, следовательно, энергия переноса углеводорода в воду с повышением температуры растет. Возрастает с увеличением температуры и свободная энергия переноса углеводорода в воду. [12]
Получено изобутана на 45 % больше, чем взято, вследствие переноса углеводорода к изобутилену. [13]
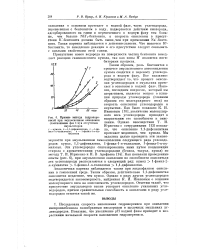 |
Кривые выхода гидроперекисей при эмульсионном окислении ( соотношение фаз в отсутствие эмульгаторов. [14] |
Таким образом, роль бентонитов в процессе эмульсионного автоокисления кумола сводится к переносу углеводорода в водную фазу. Все сказанное подтверждает то, что процесс окисления углеводородов в эмульсиях протекает в основном в водной фазе. Наконец, последним вопросом, который мы затрагиваем, является вопрос о влиянии природы углеводорода ( главным образом его молекулярного веса) на скорость окисления углеводородов в эмульсиях. Как было показано К. И. Ивановым [10], увеличение молекулярного веса углеводорода приводит к возрастанию его способности к окислению. Однако впоследствии Т. И. Юрженко с сотрудниками [13] показала, что окисление 1 1-дифенилэтана протекает медленнее, чем кумола. Мы задались целью проверить эти закономерности при эмульсионном самоокислении следующего ряда углеводородов: кумол, 1 1-дифенилэтан, 1-фенил - 1-п-толилэтан, 1-фенил - 1-п-ку - милэтан. Как показали проведенные опыты ( рис. 6), при эмульсионном окислении по способности окисляться эти углеводороды располагаются в следующий ряд: кумол 1-фенил - 2-и-кумилэтан 1-фенил - 1-п-толилэтан 1 1-дифенилэтан. [15]
Страницы: 1 2 3