Полный перенос - заряд
Cтраница 4
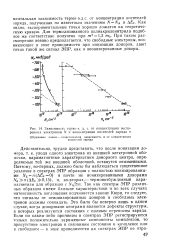 |
Зависимость термо э. д. с. от концентрации неспаренных электронов / V и концентрации носителей заряда п. [46] |
Поэтому, во-первых, должно было бы наблюдаться существенное различие в спектрах ЭПР образцов с полностью ионизированными Л / д n ( Afn 0) и почти не ионизированными донорами Л д 3 ( А. Так как спектры ЭПР различных образцов имеют близкие характеристики и во всех случаях интенсивность поглощения подчиняется закону Кюри, то следует, что сигналы от неионизированных доноров и свободных электронов должны совпадать. Это было бы неверно лишь в одном случае, когда донорными центрами являются дефекты структуры, в которых реализуются состояния с полным переносом заряда. [47]
Для сильных КПЗ характерны сдвиги полос поглощения групп СО, С - С1 и других в колебательных ИК-спектрах. Предельным случаем сильных КПЗ являются ион-радикалы с полным переносом заряда, у которых наблюдается сигнал ЭПР. При изучении КПЗ полишиффовых оснований и полиазинов с бромом и иодом установлено, что только одна из 10 - 106 молекул акцептора ( 12) Вг2) образует КПЗ с полным переносом заряда. Остальные молекулы образуют с полимером-донором сравнительно слабые КПЗ с частичным переносом заряда. [48]
Для сильных КПЗ характерны сдвиги полос поглощения групп СО, С - С1 и других в колебательных ИК-спектрах. Предельным случаем сильных КПЗ являются ион-радикалы с полным переносом заряда, у которых наблюдается сигнал ЭПР. При изучении КПЗ полишиффовых оснований и полиазинов с бромом и иодом установлено, что только одна из 10 - 106 молекул акцептора ( Ь, Вг2) образует КПЗ с полным переносом заряда. Остальные молекулы образуют с полимером-донором сравнительно слабые КПЗ с частичным переносом заряда. [49]
Образующиеся при их взаимодействии интенсивно окрашенные комплексы с переносом заряда ( я-соли) в некоторых случаях удается выделить. В результате полного переноса заряда образуется устойчивый анион-радикал, который часто удается выделить в виде относительно устойчивой соли. Так, тетрацианоэтилен ( 1008) и тетрацианохино-диметан ( 1010) восстанавливаются металлами, иодидами и третичными аминами до соответствующих анион-радикалов ( 1009) и ( 1011), дающих характерные спектры ЭПР и относительно устойчивых как в растворе, так и в виде металлических солей, которые легко можно выделить. [50]
Энергия Маделунга Ем была рассчитана для ряда солей TCNQ с сегрегированными стопками в предположении о полном переносе заряда. Результаты расчетов представлены на рис. 5.2.1, где расчетные значения Ем сравниваются с измеренными значениями разности / g - Ag. Как можно видеть, соль Na - TCNQ и две модификации соли Rb - TCNQ в соответствии с предсказанием теории, будут стабильны при значении Ем, превышающем разность Ig - Ag приблизительно на 3 эВ на молекулу, что и следовало ожидать для сильно связанных ионных солей. Таким образом, для этих солей значение энергии Маделунга свидетельствует в пользу полного переноса заряда. С другой стороны, для солей TTF - TCNQ и NMP - TCNQ предсказывается, что ионное основное состояние, соответствующее полному переносу заряда, должно быть нестабильным, так как Ем Ig - Ag. Существуют две основные причины большого различия расчетной энергии связи для солей TCNQ с щелочными металлами и солей типа TTF - TCNQ и NMP - TCNQ [152]: а) энергия ионизации TTF и NMP приблизительно на 1 5 - 2 5 эВ больше энергии ионизации доноров из щелочных металлов, и б) притягивающее кулоновское взаимодействие между противоположно заряженными стопками в соединениях щелочных металлов почти полностью компенсируется значительными силами отталкивания между одноименными зарядами внутри одной и той же стопки. [51]
На рисунке показана зависимость концентрации п.м.ц. и ширины линии от продолжительности иодирования при 250 и 350е С. Видно, что при 250 С новая линия шириной 8 э при - 196 С и 10 э при 20 С образуется только в окисленных образцах, причем в окисленных при 300 С она появляется раньше, чем в окисленных при 210 С, и что в глубоковакуумированных образцах новая линия появляется только после повышения температуры иодирования до 350 С. На тех же образцах при повышении температуры иодирования от 250 до 350 С концентрация п.м.ц. не изменяется, а ширина линии возрастает до 28 э при - 196 С и при 20 С линия не детектируется. Это означает, что и в этих продуктах, так же как в полученных при ТТО 750 С, часть иода адсорбируется без образования комплексов с полным переносом заряда, но вызывая сокращение времени спин-решеточной, релаксации имеющихся п.м.ц. из-за частичного перекрывания их орбит с орбитами иода. [52]
Мы вынуждены поэтому вновь вернуться к другой полуэмпирической трактовке. Ион - энергия взаимодействия протона и аниона А -, волновую функцию которого можно записать с помощью правил, изложенных в разделе 2.8. Вычисления такого типа могут быть выполнены с достаточной точностью. Они сравнительно просты, если только не пытаться учесть поляризацию электронного облака атома А. В кристалле NaCl атомы натрия почти полностью теряют свои валентные электроны, а атомы хлора принимают их ( см. гл. Из работ Борна ( см., например, [347, 21, 116]) известно, что при предположении такого почти полного переноса заряда удается хорошо описать свойства ионных кристаллов. При этом следует учитывать действующий между ионами потенциал притяжения e2 / R, обусловленный кулоновским взаимодействием ионов, и потенциал отталкивания b / R9 для каждой пары ионов; постоянная 6 выбирается из условия минимума полной энергии кристалла и связана с постоянной решетки. Таким способом были найдены значения Ъ для различных пар ионов. [53]
Энергия Маделунга Ем была рассчитана для ряда солей TCNQ с сегрегированными стопками в предположении о полном переносе заряда. Результаты расчетов представлены на рис. 5.2.1, где расчетные значения Ем сравниваются с измеренными значениями разности / g - Ag. Как можно видеть, соль Na - TCNQ и две модификации соли Rb - TCNQ в соответствии с предсказанием теории, будут стабильны при значении Ем, превышающем разность Ig - Ag приблизительно на 3 эВ на молекулу, что и следовало ожидать для сильно связанных ионных солей. Таким образом, для этих солей значение энергии Маделунга свидетельствует в пользу полного переноса заряда. С другой стороны, для солей TTF - TCNQ и NMP - TCNQ предсказывается, что ионное основное состояние, соответствующее полному переносу заряда, должно быть нестабильным, так как Ем Ig - Ag. Существуют две основные причины большого различия расчетной энергии связи для солей TCNQ с щелочными металлами и солей типа TTF - TCNQ и NMP - TCNQ [152]: а) энергия ионизации TTF и NMP приблизительно на 1 5 - 2 5 эВ больше энергии ионизации доноров из щелочных металлов, и б) притягивающее кулоновское взаимодействие между противоположно заряженными стопками в соединениях щелочных металлов почти полностью компенсируется значительными силами отталкивания между одноименными зарядами внутри одной и той же стопки. [54]
Терениным в 1940 г. спектроскопические исследования химии поверхности и адсорбции ведутся во многих лабораториях. Получаемая информация особо важна в случае специфической молекулярной адсорбции, для которой теория еще недостаточно разработана. Необходимо сопоставление информации о составе и состоянии поверхности ( изотопный обмен, спектры, электрофизические методы), об энергии адсорбции и вкладах в нее специфических взаимодействий и об изменениях в спектрах поверхностных соединений и адсорбированных молекул. Имеется постепенный переход от слабых специфических взаимодействий, вызывающих, однако, значительное перераспределение электронной плотности в молекулах и изменение их симметрии, до взаимодействий с полным переносом заряда. [55]
Вследствие сложности общей проблемы взаимодействий до настоящего времени еще не создано законченной теории межмолекулярных взаимодействий. Несмотря на единство квантовоме-ханической природы взаимодействий, потенциал взаимодействия обычно приближенно представляется в виде суммы вкладов взаимодействий различных типов, трактуемых как независимые. Это, во-первых, неспецифические молекулярные ван-дер-ваальсовы взаимодействия, в основном дисперсионные. Во-вторых, это специфические взаимодействия, в основном зависящие от локального распределения электронной плотности в молекуле, наличия ii-связей, свободных электронных пар. В-четвертых, это различные химические взаимодействия, в частности сильное донорно-акцепторное взаимодействие с полным переносом заряда и взаимодействия с образованием прочных ковалентных связей, когда химическая индивидуальность партнеров теряется. [56]
Негчецифическое взаимодействие универсально, оно проявляется между любыми партнерами. В основном это дисперсионное взаимодействие, связанное с согласованием движения электронов во взаимодействующих партнерах. Специфическое взаимодействие вызывается особенностями локального распределения электронной плотности на периферии взаимодействующих молекул. Эти особенности связаны с локальным концентрированием отрицательного и положительного зарядов на периферии отдельных связей или звеньев специфически взаимодействующих партнеров. Эти взаимодействия в общем не классические и только в предельных случаях достаточно больших расстояний они сводятся к классическим электростатическим взаимодействиям. Водородная связь представляет собой частный случай таких специфических, но еще молекулярных взаимодействий. Наконец, еще более тесные взаимодействия, например взаимодействия с полным переносом заряда между партнерами, как при возникновении донорно-ак - Цепторной координационной химической связи, приводят к потере - - химической индивидуальности взаимодействующих партнеров. Од - чним из характерных примеров такого взаимодействия является адсорбция антрацена на алюмосиликатном катализаторе [6], ( N. [57]
Несчецифическое взаимодействие универсально, оно проявляется между любыми партнерами. В основном это дисперсионное взаимодействие, связанное с согласованием движения электронов во взаимодействующих партнерах. Специфическое взаимодействие вызывается особенностями локального распределения электронной плотности на периферии взаимодействующих молекул. Эти особенности связаны с локальным концентрированием отрицательного и положительного зарядов на периферии отдельных связей или звеньев специфически взаимодействующих партнеров. Эти взаимодействия в общем не классические и только в предельных случаях достаточно больших расстояний они сводятся к классическим электростатическим взаимодействиям. Водородная связь представляет собой частный случай таких специфических, но еще молекулярных взаимодействий. Наконец, еще более тесные взаимодействия, например взаимодействия с полным переносом заряда между партнерами, как при возникновении донорно-ак - Л цепторной координационной химической связи, приводят к потере химической индивидуальности взаимодействующих партнеров. Од - ] ним из характерных примеров такого взаимодействия является ч адсорбция антрацена на алюмосиликатном катализаторе [6], декатионированном цеолите [7] и двуокиси алюминия [8], при TV. [58]
Страницы: 1 2 3 4