Прямой перенос - электрон
Cтраница 1
Прямой перенос электрона с атома Ме2 на Mei в данном случае невозможен. [1]
Это достигается прямым переносом электронов в случае ионной связи или участием соответствующих электронов в ковалентных связях. Исходя из стабильности электронной структуры благородных газов, в течение длительного времени считали, что соединения этих газов существовать не могут. [2]
Очевидно, что прямой перенос электрона крайне медленный. [3]
На первой стадии происходит либо прямой перенос электронов от электрода к данному органическому соединению, либо образование сольватированных электронов, либо разряд атомов водорода у поверхности электрода. Какой именно будет первая стадия и что последует дальше - это зависит, очевидно, от ряда факторов. Важную роль играет природа растворителя - применяются и водные, и безводные, и смешанные растворители. Растворитель не только влияет на первую стадию, но и изменяет состав адсорбированного слоя на поверхности электрода и вступает в химическую реакцию с образованием неустойчивого промежуточного продукта. Электрод может оказывать влияние на реакцию благодаря своей каталитической активности, а также адсорбционной способности по отношению к различным атомам и молекулам, имеющимся в растворе. Очень важное значение имеет также его водородное перенапряжение: если рассматриваемое соединение восстанавливается с трудом, то на металлическом электроде с низким перенапряжением будет выделяться водород и лишь электрод с высоким перенапряжением будет обеспечивать подвод энергии, необходимой для восстановления. Образование продукта реакции зависит также от таких факторов, как концентрация органического соединения, плотность тока, скорость перемешивания, температура, наличие в электролите кислотных, щелочных или других катализаторов, например солей титана или церия. [4]
 |
Схематическое изображение гальванического элемента. [5] |
Окислительно-восстановительные реакции могут происходить вследствие прямого переноса электронов от донора к акцептору. [6]
Первичное электрохимическое восстановление или окисление путем прямого переноса электронов от катода к субстрату или от субстрата к аноду-осуществляется с практически значимой скоростью только начиная с некоторого значения электродного потенциала. Для обратимых электрохимических окислительно-восстановительных реакций, которые в случае органических реакций являются скорее исключением, это значение должно быть близким к соответствующему нормальному электродному потенциалу. При более положительных потенциалах происходит окисление восстановленной формы, при более отрицательных - восстановление окисленной формы соответствующего субстрата. [7]
В этой главе обсуждаются только случаи прямого переноса электрона с катода к молекуле органического вещества. Непрямое электровосстаиовление с использованием гомогенного пе реноса электрона с электрохимически генерированного интер-медиата на галогенид рассматривается в гл. [8]
Судьба CN, образующегося в результате прямого переноса электрона с CN - на катион-радикал ТАА, неизвестна. [9]
Это более устойчивое расположение электронов может быть достигнуто тремя путями: 1) прямым переносом электронов ( окисление-вос. Лишь второй из этих трех путей требует здесь дальнейшего обсуждения. Новые координационные коваленгные связи могут образоваться двумя путями: 1) нейтрализацией, разобранной в гл. [10]
Раскрытие механизма окислительно-восстановительного процесса означает, что получены ответы на следующие вопросы: происходит ли прямой перенос электрона или он протекает за счет переноса атома; какие атомы переносят электроны; через какие промежуточные состояния осуществляется процесс. Результаты экспериментальных исследований не всегда удается однозначно интерпретировать, и, следовательно, выводы о механизме окисления-восстановления часто являются предположительными. [11]
 |
Окислительные потенциалы галогенид-ионов. [12] |
В работе ( [4] была исследована кинетика реакции катион-радикала перилена с галогенид-ионами, из чего был сделан вывод, что только иодид-ион восстанавливает катион-радикал путем прямого переноса электрона. [13]
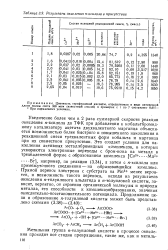 |
Результаты окисления п-ксилола в присутствии. [14] |
Прямой перенос электрона с субстрата на Мп3 менее вероятен, и возможность такого переноса, исходя из результатов окисления л-толуилового альдегида и л-толуиловой кислоты, зависит, вероятно, от строения органической молекулы и природы металла, его способности к комплексообразованию, значения окислительно-восстановительного потенциала. [15]
Страницы: 1 2 3