Переориентация - молекула - растворитель
Cтраница 1
Переориентация молекул растворителя является четвертым фактором, который также должен иметь определенное значение. Если образование переходного состояния приводит к изменению числа или величины ионных зарядов или к изменению распределения заряда, то можно ожидать переориентации молекул растворителя. [1]
Переориентация молекул растворителя или лигандов - процесс сложный и сравнительно медленный. В этом случае скорость переноса электрона будет определяться скоростью реорганизации молекул растворителя или лигандов. Далее, перенос электрона от одного иона к другому может облегчаться, когда ядра комплексных ионов оказываются в непосредственной близости одно от другого. При этом разделяющий их барьер сужается, что должно способствовать как переносу электрона через барьер, так и туннельному просачиванию. В соответствии с принципами квантовой механики, эти теории рассматривают электрон не как дискретную частицу, а оперируют с распределением электронной плотности, которая непрерывно меняется по мере осуществления процесса, выражаемого схемой AZA - - AZA - x % е -, где % возрастает от нуля до единицы. [2]
Переориентация молекул растворителя или лигандов - процесс сложный и сравнительно медленный. В этом случае скорость переноса электрона будет определяться скоростью реорганизации молекул растворителя или лигандов. Далее, перенос электрона от одного иона к другому может облегчаться, когда ядра комплексных ионов оказываются в непосредственной близости одно от другого. При этом разделяющий их барьер сужается, что должно способствовать как переносу электрона через барьер, так и туннельному просачиванию. В соответствии с принципами квантовой механики, эти теории рассматривают электрон не как дискретную частицу, а оперируют с распределением электронной плотности, которая непрерывно меняется по мере осуществления процесса, выражаемого схемой A A - A2A - X уе -, где % возрастает от нуля до единицы. [3]
После возбуждения начинается переориентация молекул растворителя, и система приближается к равновесию со средой. Величина этого смещения, а также степень равновесности системы определяются соотношением средних времен пребывания молекул в возбужденном состоянии т и переориентации ( релаксации) частиц окружения тг. При комнатной температуре ту имеет порядок Ш Ч - Ю 12 с; для разрешенных переходов многих органических молекул т 10 - 8 с. В этом случае за время возбужденного состояния практически все молекулы растворителя переориентируются и установится их стабильная конфигурация. [4]
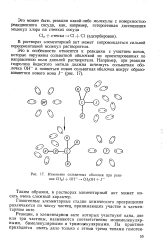 |
Изменение сольватных оболочек при реакции CH3J ОНГ - СН3ОН J. [5] |
В растворах элементарный акт может сопровождаться сильной переориентацией молекул растворителя. [6]
 |
Изменение сольватных оболочек в реакции СН31 ОН - - СН3ОН. 1. [7] |
Например, в растворах элементарный акт может сопровождаться сильной переориентацией молекул растворителя. Это особенно относится к реакциям с участием ионов, которые окружены сольватной оболочкой из ориентированных по направлению поля иона диполей растворителя. [8]
В можно разделить на вклады отдельных ионов ( В), которые линейно зависят от относительных времен переориентации молекул растворителя, связанных с каждым из ионов. Если числа сольватации неизвестны, то нельзя определить и эти времена, однако ясно, что положительные В соответствуют возрастанию времени изменения ориентации молекул растворителя. Времена переориентации убывают в рядах С1 - Вт - 1 - и Li Na K Rb Cs, В органических растворителях частота вращения ( переориентации) в меньшей степени зависит от радиуса иона, чем в воде. В этих растворителях не обнаружено проявлений отрицательной сольватации. Во всех случаях времена переориентации, рассчитанные для равных количеств сольватных молекул, связанных с каждым из ионов, больше, чем в воде, однако не столь велики, как можно было бы ожидать для жестких сольватных оболочек. [9]
Это явление объяснено тем, что сольватация ионной пары облегчается с понижением устойчивости структуры растворителя, так как последнее ведет к меньшим энергетическим затратам на переориентацию молекул растворителя при их взаимодействии с ионной парой. [10]
Сравнение энергии активации переориентации и энергии активации вязкого течения показывает, что для этих растворов так же, как и для чистого растворителя, всегда выполняется соотношение Ui Ut. Это свидетельствует о том, что переориентация молекул растворителя происходит с большей вероятностью не во время трансляционного движения, а во время колебаний молекул около положений равновесия. [11]
В жидкой фазе и на границе раздела фаз элементарный акт может сопровождаться изменением состояния близлежащих частиц, не претерпевающих химического превращения. Например, в растворах элементарный акт может сопровождаться переориентацией молекул растворителя, окружающих реагирующие частицы. [12]
Переориентация молекул растворителя является четвертым фактором, который также должен иметь определенное значение. Если образование переходного состояния приводит к изменению числа или величины ионных зарядов или к изменению распределения заряда, то можно ожидать переориентации молекул растворителя. [13]
Сольватационный и гидрофобный вклады минимальны и близки к нулю. Однако они, видимо, не учли, что образование полости в структуре воды ( или другого растворителя) неизбежно сопряжено с переориентацией молекул растворителя и изменением их взаимного расположения, т.е. с перестройкой структуры растворителя. Иными словами, полостной и структурный вклады, по сути дела, неразрьшно связаны друг с другом и должны рассматриваться как единый конфигурационный вклад. К этому нужно добавить, что само существование полостного вклада в термодинамические характеристики растворения неполярных веществ в воде является весьма проблематичным. [14]
В общем случае, однако, замораживание равновесий не обязательно должно быть связано с сильным различием энтропии начального и конечного состояний реакции. К подобным эффектам может приводить изменение дипольного момента и, следовательно, энтропии системы в промежуточных областях координаты реакции, в частности в области активационного барьера. Можно, вообще говоря, представить себе и такую ситуацию, когда дипольный момент комплекса или молекулы в ходе реакции не меняется ( или почти не меняется) по величине, но зато меняется его направление. Энтропия системы в этом случае не меняется, однако возможность переориентации молекул растворителя зависит от вязкости среды, и равновесие может заморозиться. [15]
Страницы: 1 2