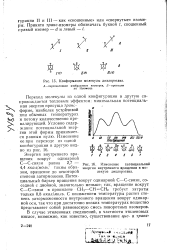
Переход - молекула
Cтраница 1
Переход молекул из возбужденного состояния в нормальное протекает различными путями. [1]
Переход молекул вследствие их теплового движения из одного слоя в другой в ламинарном потоке сопровождается переносом количества движения. Переход молекул из слоя, движущегося быстрее, в слой, движущийся медленнее, приведет к ускорению движения этого слоя и, наоборот, попадание в быстро движущийся слой молекул из медленно движущегося будет замедлять движение первого слоя. Между этими слоями происходит процесс внутреннего трения. [2]
Переход молекул может быть вызван действием сил, которые мы до сих пор оставляли без внимания. Действие сил тяжести незначительно и им можно пренебречь. Напротив, влияние электрических полей следует рассмотреть. Последние постоянно действуют, если фазовый переход происходит с участием ионов, как, например, при электролизе и при построении или декристаллиза-ции гетерополярной решетки. [3]
Переход молекул из подвижной фазы в неподвижную называют сорбцией, а обратный переход - десорбцией. [4]
Переход молекул газе в раствор характеризуется уменьшением кинетической энергии молекул газа, которая передается молекулам жидкости, уравнивая общую энергию смеси. Это явление сопровождается выделением теплоты абсорбции. [5]
Переход молекул из основного в электронно-возбужденные состояния в растворе происходит как быстро по сравнению со скоростями их вращательного и поступательного движения, что расположение соседних молекул растворителя, противоионов и других растворенных веществ вокруг возбужденной частицы остается таким же, как в основном состоянии. Однако электронная структура может быть сильно возмущена. Часто происходят значительные изменения в дипольных моментах. [6]
Переход молекул между струями газа, движущимися с разными скоростями, создает силу трения, которая действует на газ и соответственно на макроскопическую частицу. Для вычисления этой силы необходимо знать распределение по скоростям для струй газа, обтекающего частицу. [7]
Переход молекулы с верхнего вращательного энергетического уровня на нижний приводит к возникновению линии вращательного спектра испускания. [8]
Переход молекулы между двумя электронными уровнями сопровождается многими сопутствующими переходами между колебательными уровнями. [9]
Переход молекулы из глубины жидкости в поверхностный слой связан с необходимостью совершения работы против действующих в поверхностном слое сил. Эта работа совершается молекулой за счет запаса ее кинетической энергии и идет на увеличение потенциальной энергии молекулы, подобно тому как работа, совершаемая летящим вверх телом против сил земного тяготения, идет на увеличение потенциальной энергии тела. При обратном переходе молекулы в глубь жидкости потенциальная энергия, которой обладала молекула в поверхностном слое, переходит в кинетическую энергию молекулы. [10]
Переход молекулы из одной конфигурации в другую сопровождается тепловым эффектом: минимальная потенциальная энергия присуща трансформе, наиболее устрйчивой ппи обычных температурах и потому количественно превалирующей. Условно содержание потенциальной энергии этой формы принимается равным нулю. [12]
 |
Две возможные конфигурации SiF4. [13] |
Переходы молекулы из одной высокосимметричной конфигурации в твердом состоянии в другую, также с высокой, но иной симметрией, в газе наблюдаются очень редко. [14]
Переход молекул из жидкости в пар называется испарением. Обратный переход молекул из пара в жидкость называется конденсацией. Ясно, что число конденсирующихся молекул пропорционально плотности молекул в паре. Поэтому, если сосуд закрыт, то непременно наступит момент, когда число частиц, покидающих в единицу времени жидкость, станет равным числу частиц, возвращающихся за это же время в жидкость. [15]
Страницы: 1 2 3 4