Переход - молекула - вода
Cтраница 3
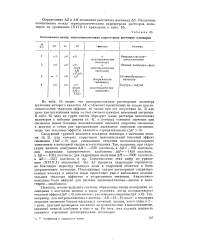 |
Соотношения между термодинамическими параметрами растворов полимеров. [31] |
Так, например, при гидратации яичного альбумина АЯ - 1570 кал / моль, a AZ-892 кал / моль; для гидратации сывороточного альбумина АЯ-1450 кал / моль, a AZ-1034 кал / моль; для гидратации желатины АЯ-3800 кал / моль, a AZ - 1537 кал / моль и др. Сопоставление этих цифр по уравнению ( XVIII1) показывает, что АЛ1 процесса гидратации отрицательно благодаря переходу молекул воды в гидратной оболочке в более упорядоченное состояние. Последующая стадия растворения гидратиро-ванных молекул в избытке воды происходит уже с небольшим положительным тепловым эффектом и возрастанием энтропии. Аналогичное поведение было найдено для системы ацетилцеллюлоза-ацетон и полистирол - этилбензол. [32]
Из наружного сосуда вода будет проходить во внутренний и подниматься по трубке, соединенной с внутренним сосудом. При этом будет повышаться гидростатическое давление, под которым находится раствор во внутреннем сосуде. Вследствие этого скорость перехода молекул воды из внутреннего сосуда в наружный увеличивается. Наконец - при некоторой высоте h столба раствора в трубке скорости прохождения воды из наружного сосуда во внутренний и из внутреннего в наружный сравняются, и подъем жидкости в трубке прекратится. Давление, которое отвечает такому равновесию, может служить количественной характеристикой явления осмоса. Оно называется осмотическим давлением. Про - нужно приложить к раствору, чтобы привести его в равнове-стейший прибор, сие с чистым растворителем, отделенным от него полупрони-для определе -, цаемой перепонкой. [33]
 |
Простейший прибор для определения осмотического давления. [34] |
Из наружного сосуда вода будет проходить во внутренний и подниматься по трубке, соединенной с внутренним сосудом. При этом будет повышаться гидростатическое давление, под которым находится раствор во-внутреннем сосуде. Вследствие этого скорость перехода молекул воды из внутреннего сосуда в наружный увеличивается. Наконец, при некоторой высоте h столба раствора в трубке скорости прохождения воды из наружного сосуда во внутренний и из внутреннего в наружный сравняются, и подъем жидкости в трубке прекратится. Давление, которое отвечает такому равновесию, может служить количественной характеристикой явления осмоса. Оно называется осмотическим давлением. Таким образом, осмотическое давление равно тому давлению, которое нужно приложить к раствору, чтобы привести его в равновесие с чистым растворителем, отделенным от него полупроницаемой перепонкой. [35]
 |
Осмотическое давление я ( в бар раствора сахара различной концентрации е ( в моль / л при О С. [36] |
Из на - ружного сосуда вода будет проходить во внутренний и подниматься по трубке, соединенной с внутренним сосудом. При этом будет повышаться гидростатическое давление, под которым находится раствор во внутреннем сосуде. Вследствие этого скорость перехода молекул воды из внутреннего сосуда в наружный увеличивается. Наконец, при некоторой высоте h столба раствора в трубке скорости прохождения воды из наружного сосуда во внутренний и из внутреннего в наружный сравняются, и подъем жидкости в трубке прекратится. Давление, которое отвечает такому равновесию, может служить количественной характеристикой явления осмоса. Оно называется осмотическим давлением. Таким образом, осмотическое давление равно тому давлению, которое нужно приложить к раствору, чтобы привести его в равновесие с чистым растворителем, отделенным от него полупроницаемой перепонкой. [37]
В зависимости от условий может происходить не только укрупнение капелек воды, образовавшихся в топливе, но и растворение их в топливе. Если испарение капель воды, образовавшихся в атмосфере, возможно только в результате повышения температуры воздуха, то в топливе они могут растворяться не только при повышении температуры топлива, но и при постоянной его температуре или при ее понижении. Объясняется это возможностью перехода молекул воды из топлива в воздух, с которым соприкасается топливо, в тех случаях, когда воздух оказывается более сухим, чем топливо. Так, если прибывшее в железнодорожной цистерне помутневшее топливо ( топливо, содержащее капельки воды) перекачать в резервуар, в котором воздух имеет небольшую относительную влажность, то переход молекул воды из топлива в воздух будет происходить независимо от изменения температуры топлива. [38]
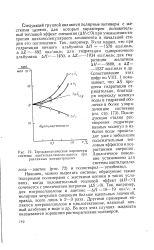 |
Термодинамические параметры. [39] |
Следующей группой являются полярные полимеры с жесткими цепями, для которых характерен положительный тепловой эффект смешения ( ДЯ0) при уменьшении энтропии низкомолекулярного компонента в начальной стадии его поглощения. Так, например, Булл нашел, что при гидратации яичного альбумина ДЯ - 1570 кал / моль, a AZ-892 кал / моль; для гидратации сывороточного альбумина ДЯ - 1450, a AZ-1034 кал / моль; для гидратации желатины ДЯ-3800, a AZ - 1537 кал / моль и др. Сопоставление этих цифр по VIII. AS процесса гидратации отрицательно, благодаря переходу молекул воды в гидратной оболочке в более упорядоченное состояние ( см. стр. Последующая стадия растворения гидратиро-ванных молекул в избытке воды происходит уже с небольшим положительным тепловым эффектом и возрастанием энтропии. Аналогичное поведение установлено для системы ацетилцеллю-лоза - ацетон ( рис. 72) и полистирол - зтилбензол. [40]
Бывают и другие виды изомерии комплексных соединений. Так, ион, находящийся в одной координационной сфере, например во внешней, может обменяться местом с ионом, который помещается во внутренней сфере, при этом получатся два ионных изомера. Это явление называется ионизационной изомерией. К нему близко примыкает и гидратная изомерия, для которой характерен переход молекул воды из одной сферы в другую. Известны гидратные изомеры комплексов хрома: [ Сг ( Н2О) е ] С1з, окрашенный в светло-фиолетовый цвет, и [ Сг ( Н2О) 4СЬ ] С1 зеленого цвета. [41]
В зависимости от условий может происходить не только укрупнение капелек воды, образовавшихся в топливе, но и растворение их в топливе. Если испарение капель воды, образовавшихся в атмосфере, возможно только в результате повышения температуры воздуха, то в топливе они могут растворяться не только при повышении температуры топлива, но и при постоянной его температуре или при ее понижении. Объясняется это возможностью перехода молекул воды из топлива в воздух, с которым соприкасается топливо, в тех случаях, когда воздух оказывается более сухим, чем топливо. Так, если прибывшее в железнодорожной цистерне помутневшее топливо ( топливо, содержащее капельки воды) перекачать в резервуар, в котором воздух имеет небольшую относительную влажность, то переход молекул воды из топлива в воздух будет происходить независимо от изменения температуры топлива. [42]
Если сосуд с раствором какого-либо вещества отделен от сосуда с растворителем ( водой) мембраной, проницаемой только для молекул растворителя, то наблюдается перемещение молекул растворителя через мембрану в раствор. Такой самопроизвольный переход молекул растворителя через полупроницаемую мембрану называется осмосом. Если концентрации растворов, разделенных мембраной, равны, наступает равновесие, характеризующееся одинаковой скоростью перехода молекул воды в тот и другой растворы. [43]
Страницы: 1 2 3