Переход - внешний электрон
Cтраница 1
Переходы внешних электронов в атомах сопряжены с меньшими энергетическими изменениями и обусловливают излучение в видимой и УФ-областях. [1]
Переходы внешних электронов в атомах сопряжены с меньшими энергетическими изменениями и обусловливают возникновение спектра в видимой и ультрафиолетовой областях. [2]
Следующее столкновение с электроном обусловливает переход внешних электронов иона аргона ( Аг) в одно из нескольких 4р - состояний, в результате последующего перехода в 45-состояние возникает линия излучения. Таким образом, переходы между различными уровнями в 4р - и 45-состояниях сопровождаются излучением при 4880, 4965 и 5145 А. [3]
С точки зрения квантовой теории излучение вызывается переходом внешних электронов атомов излучающего тела на орбиты меньшего энергетического уровня с выделением квантов энергии излучения. [4]
Образование ионной молекулы при сближении атомов осуществляется путем перехода внешних электронов от электроположительных к электроотрицательным атомам с образованием соответственно положительных и отрицательных ионов этих атомов. [5]
С другой стороны, в низкоспиновом комплексе [ Mnn ( CN) e ] 2 - при переходе внешнего электрона на уровень tzg происходит выигрыш энергии. [6]
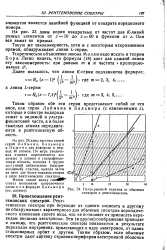 |
Непрерывный переход от обычных спектров к рентгеновским. [7] |
Рентгеновские спектры при переходе от одного элемента к другому не обнаруживают характерного для обычных спектров периодического изменения своего вида, что не позволяет их приписать переходам внешних электронов. Эти ( и другие) соображения приводят к выводу, что рентгеновские спектры появляются в результате переходов внутренних, прилегающих к ядру электронов, от одних стационарных орбит к другим. [8]
Характеристические рентгеновские лучи возникают при отрыве электронов с К -, L - и ЛГ-оболочек атома с последующим возвращением атома из возбужденного состояния в нормальное путем перехода внешних электронов на вакантные места внутренних оболочек. Атомы с определенным атомным номером излучают строго определенные по длинам волн рентгеновские фотоны. [9]
В jfsT - оболочке или в другой внешней оболочке ( в зависимости от энергии падатощего электрона или фотона) появляется свободное место. В результате перехода внешнего электрона на освободившееся место и возникает характеристическое рентгеновское излучение. [10]
Одноатомные газы характеризуются линейчатыми спектрами. Спектры резкой абсорбции ( линейчатые спектры) атомов определяются переходом внешних электронов атомов с основного энергетического уровня на верхние дискретные уровни. Такое поглощение принято называть резонансным. Типичным примером резонансной линии является линия ртути 253 67 А. [11]
Первое слагаемое в уравнении ( 24 - 1), как правило, больше двух других, и для переходов внешних электронов обычно требуется энергия видимого и УФ-излучений. В этом случае каждому электронному состоянию соответствует множество колебательных и вращательных энергетических состояний. При данном значении ЕЭ31 величина Е будет мало меняться с изменением Екол и ЕВр или обоих вместе. Если используемый прибор не обладает высоким разрешением, отдельные полосы сливаются, в результате спектр получается в виде плавной кривой. [12]
Неупругие столкновения электронов с атомами могут вызывать их ионизацию, в результате чего возникают характеристические рентгеновские лучи. Характеристическое рентгеновское излучение является следствием отрыва электронов с К -, L - и Af-оболочек атома с последующим возвращением атома из возбужденного состояния в нормальное путем перехода внешних электронов на вакантные места внутренних оболочек. В силу этого длины излучаемых волн для каждого химического элемента имеют строго определенные значения. Основное назначение МРА - качественное и количественное определение химического состава приповерхностных слоев. Локальность анализа по объему составляет несколько кубических микрометров. [13]
Большинство спектров, наблюдаемых обычно в видимой или ультрафиолетовой областях, обусловлены возбуждением одного или, реже, двух электронов на наименее стабильной внешней орбите атома или иона. Заполненные внутренние слои орбит атома называются остовом. На электроны остова мало влияют переходы внешних электронов, но электроны остова могут быть возбуждены при бомбардировке частицами с большой энергией или при поглощении рентгеновских лучей. [14]
Каждый элемент в своем периоде является предпоследним d - элементом. Таким образом, в атомах этих элементов в ( и - ) d - оболочке должно находиться 9 электронов, но поскольку d - оболочка близка к завершению, энергетически более выгодным оказывается переход одного из s - электронов наружного слоя в ( п - 1) й-оболочку Поэтому Си, Ag и Аи имеют электронную конфигурацию... Поскольку завершение d - оболочки у этих элементов происходит за счет перехода внешнего электрона, rf - оболочка еще недостаточно стабильна. Поэтому в образовании химических связей у элементов подгруппы меди могут принимать участие и d - электроны. Серебро в, соединениях, главным образом одновалентно. Соединения Си в степени окисления 3, Ag ( 2 и 3) и Аи ( 2) гораздо менее устойчивы и хуже изучены. [15]
Страницы: 1 2