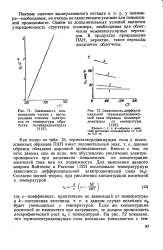
Межмолекулярный переход
Cтраница 1
Межмолекулярные переходы становятся более интенсивными при повышении давления, под действием ионизирующей радиации, при введении в пирополимеры металлов и галогенов. Дополнительная возможность таких переходов появляется при ориентации полимерных полупроводников. Так, увеличение степени вытяжки волокон из ПАН от 2 до 25 приводит к росту электрической проводимости примерно на порядок. Кристаллизация полиацетиленов и продуктов термообработки диэтилбензола также сопровождается увеличением проводимости. Путем термообработки получены электропроводящие полимеры с полупроводниковыми свойствами из ПАН, полифенила, поливинилиденхлорида и других полимеров. [1]
Важность вопроса о межмолекулярных переходах легко видеть из того, например, факта, что в то время как молекула бензола является прекрасным проводником, совокупность этих молекул - жидкий бензол - является прекрасным изолятором. [2]
Такой парамагнетизм этих соединений, по-видимому, является следствием межмолекулярных переходов электронов от атома никеля к молекуле хинона; это означает, что связь никель-хинон содержит и полярную и ковалентную компоненту. Следовательно, эти сильно выраженные парамагнитные комплексы, особенно комплексы с диметилхинонами, следует в дальнейшем рассматривать не как комплексы нульвалентного никеля, по крайней мере в твердом состоянии, а как соединения, содержащие никель в промежуточном между N1 ( 0) и N1 ( 11) состоянии окисления. [3]
Одним из дополнительных условий является упорядоченность структуры полимера, необходимая для облегчения межмолекулярных переходов. В продуктах превращения ПАН, вероятно, такие переходы достаточно облегчены. [5]
Кроме того, результаты исследования электрохромизма могут служить прямым доказательством наличия внутри - и межмолекулярных переходов с переносом заряда. [6]
А-мера интенсивности излучения молекулы А, выраженная в тех же единицах, что и коэффициент поглощения; ев - молярный коэффициент поглощения молекул В; пАв - число межмолекулярных переходов за 1 сек. A; N - число Авогадро ( рассчитанное на миллимоль); R-расстояние между молекулами. [7]
Результаты показали, что а) карбинольная группа этанола переходит в альдегидную группу ацетальдегида, б) атомы водорода от триметиламинной группы не отщепляются, в) атомы водорода этанола весьма подвижные и г) происходит межмолекулярный переход атомов водорода. [8]
 |
Физические и каталитические свойства карбонилов металлов VI-VIII групп при изомеризации гептенов. [9] |
Мануэль [42] наблюдал цис-транс-изоыернза-цию стильбена в присутствии Рез ( СО) 12, хотя молекула стильбена не содержит аллильного водорода, который мог бы участвовать в образовании гидрокарбонила. Поскольку скорости изомеризации в присутствии НСо ( СО) 4 и DCo ( CO) 4 были близки, полученные данные указывают на малую вероятность межмолекулярного перехода аллильного водорода от олефина к карбонилу. [10]
Две общих закономерности наблюдаются для изотопного перераспределения на N10 или N10 - Si02 и димеризации на N10 - Si02, а именно: 1) активность катализатора в обеих реакциях подавляется следами окиси углерода и 2) в обеих реакциях реакционная способность этилена выше, чем пропилена. Это предполагает близкое соответствие между механизмами двух реакций. Активные центры в обеих реакциях представляются сходными. Аналогия активных центров возможна только в том случае, если считать, что обе реакции включают межмолекулярный переход водорода. [11]
Здесь следует различать два вопроса: во-первых, как зарождаются носители тока и, во-вторых, каким образом они перемещаются в объеме твердого тела. Механизм возникновения носителей в сопряженных системах не вызывает особых трудностей для понимания. Зарождение носителей тока должно достаточно легко происходить на участках полимера с высокой степенью сопряжения, поскольку с ростом числа сопряженных связей снижается внутримолекулярный барьер для переброса электрона на свободные уровни молекулы и, следовательно, ослабевает возбуждение электрона при переходе в квазисвободное проводящее состояние внутри молекулы. Действительно, опытами по измерению проводимости на переменном токе показано, что энергия зарождения носителей внутри области сопряжения близка к нулю и уж во всяком случае значительно меньше энергии межмолекулярных переходов. [12]
 |
Катализ твердого вещества твердым веществом. [13] |
Существование свободных электронов в металлическом катализаторе не всегда может служить объяснением каталитического действия металлов. Каталитическая активность может быть связана с явлением электронной изомерии. Свинне [249] утверждает, что металлическая поверхность образована различными группами электронов, каждая группа имеет одинаковое общее число электронов и соответствующее ей атомное ядро. В зависимости от того, принадлежат ли эти электроны атомам, способным диссоциациирсвать на ионы и электроны или неспособным диссоциировать, возникают активные или пассивные изомеры. В то время как активный изомер диссоциирует на ионы и электроны, пассивный изомер не обладает настоящими валентными электронами, способными переходить в свободное состояние. Различные вещества, в том числе и катализаторы, могут быть причиной превращения одного электронного изомера в другой, сопровождающегося межмолекулярными переходами электронов. [14]
Особый интерес представляли превращения аг - - тетралилметилсуль-фида [12], в котором с одной из валентностей серы связан простейший радикал - метил. Соединения, содержащие в своем составе метальную группу, часто отличаются от высших гомологов особыми свойствами. В катализате этого сульфида и в отходящих газах были найдены два тиола, ar - - тиотетралол и метилмеркап-тан. Наличие их в продуктах катализа говорит о том, что разрыв молекул тетралилметилсульфида также происходит по обеим связям серы с радикалами. Однако, в отличие от высших гомологов, при распаде тетралилметилсульфида по связи серы с метилом, ввиду отсутствия водорода в ( 3-положении к сере, вместо внутримолекулярного перехода его наблюдается межмолекулярный переход. В этом и заключается специфичность превращений аг - [ 3-тетралилметилсульфида. Особое место занимает также и аг - - тетралил-фенилсульфид. В отличие от предыдущих смешанных сульфидов тетралина, распад этого соединения происходит только по одной связи серы с тетрали-новым радикалом; распад по связи серы с фенилом, по-видимому, не имеет места, поскольку в катализате был найден тиофенол ( около 40 %) и не обнаружено даже следов бензола. [15]
Страницы: 1 2