Первый короткий период
Cтраница 2
Далее фтор ( 2 9) имеет конфигурацию Is 22s22pl2p22pz и неон ( Z - 10) - конфигурацию ls22s22p22p22 / 72, причем все орбитали с низкой энергией оказываются заполненными. Ряд элементов от лития до неона называется первым коротким периодом. [16]
Остальные элементы группы IVB аналогичных соединений не образуют. Эти соединения включают л-связи, а только у элементов первого короткого периода эти связи прочные ( разд. [17]
Формулы простейших молекулярных гидридов ( кроме гидридов бора, представляющих исключение) имеют вид АН8 v, где N обозначает номер группы периодической системы. Образование 8 - Л связей приводит к группе, состоящей из восьми электронов, которые в элементах первого короткого периода заполняют вторую квантовую группу. [18]
Поскольку у элементов первого короткого периода имеется только четыре орбиты, они не могут давать более четырех ковалентных связей ни в виде нейтральных атомов, ни при потере или присоединении электронов. В следующих периодах разность энергий между самыми внешними s - и р-орбитами и следующими за ними более высокими орбитами становится, однако, значительно меньше, чем в первом коротком периоде, и вследствие этого такие более высокие орбиты также могут использоваться для образования связей. [19]
Некоторые лантаниды встречаются и в других состояниях окисления, хотя эти состояния всегда менее устойчивы, чем состояние, характерное для группы. Наличие состояний окисления II и IV в какой-то мере можно связать с электронным строением, если предположить, что вакантная, заполненная наполовину и заполненная полностью / - оболочки обладают особой устойчивостью. Такое же явление ( хотя и в меньшей степени) наблюдается в обычных рядах переходных элементов ( особенно у Мп) и для потенциалов ионизации первого короткого периода ( ср. Так, Sc, Y и La образуют только ионы М3, поскольку удаление у них трех электронов приводит к образованию конфигурации инертного газа. Lu и Gd также образуют только ионы М3, но уже потому, что эти ионы имеют устойчивую конфигурацию 4 / 14 и 4 / 7 соответственно. [20]
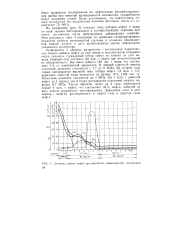 |
Динамика добычи нефти при разработке макропористых коллекторов. [21] |
Особенность I периода разработки - интенсивное наращива-нне темпов добычи нефти за счет ввода в эксплуатацию большого числа скважин. Все было добыто 150 тыс. т воды, что составляет 5 % от извлеченной продукции. В первый короткий период пластовое давление снижается с 7 7 до 6 МПа. Пластовое давление снижается до 4 МПа. На 1 млн. т добытой нефти за I период ( за 2 года) расходуется пластовой энергии порядка 0 7 МПа. Таким образом, почти за 2 года извлекается свыше 4 млн. т нефти, что составляет 45 % нефти, добытой за весь период разработки месторождения. [22]
В случае азота и кислорода нет необходимости при образовании связей промотировать какие-либо электроны, так как эти атомы имеют соответственно три или два неспаренных электрона в их основных состояниях: 2s2 2рх 2ру 2рг для азота и 2s2 2pl 2p y 2p z для кислорода. Такие соединения невозможны, если основываться на простых представлениях об октетах, когда критерием устойчивости считается возникновение конфигурации инертного газа, но при рассмотрении орбит их нельзя просто исключить. При этом заняты пять или шесть орбит вокруг азота и кислорода, тогда как во второй квантовой оболочке имеются всего четыре. Следующими за ними орбитами с минимальной энергией являются орбиты 3s и Зр, но для возбуждения электронов на эти орбиты с целью образования связей требуется гораздо больше энергии, чем можно выиграть за счет дополнительных связей. Такой вывод справедлив для всех атомов первого короткого периода, и ни один из них не образует более четырех ковалентных связей. Таким образом, элементы от лития до фтора подчиняются правилу октета. У водорода, имеющего только ls - орбиту, которая может быть использована без большой затраты энергии, максимальная ковалентность равна, очевидно, единице, что согласуется с опытом. Однако вокруг атома могут присутствовать и менее восьми валентных электронов; так, например, азот может образовать не три связи, а только одну. В действительности такое положение осуществляется редко; если только возможно, образуется полный октет электронов, так как при этом возникает больше связей, выделяется больше энергии и, следовательно, образующееся соединение более стабильно. [23]
Иногда говорят о диспергирующих присадках, которые обеспечивают якобы уменьшение размера частиц осадка. Такие присадки не диспергируют уже образовавшиеся крупные частицы осадка или отложения, а предотвращают или ограничивают укрупнение частиц до недопустимых размеров. Однако по отношению к топливным системам, ранее загрязненным отложениями, подобные присадки, введенные с топливом, будут играть диспергирующую ( моющую) роль до тех пор, пока система не будет очищена от загрязнений. Проникая в толщу более или менее плотно слежавшегося пористого слоя загрязнений, поверхностно-активная присадка будет обволакивать частицы загрязнений, расчленяя их тем самым на составляющие агрегаты, выносимые потоком топлива из системы. Это подтверждается усиленным засорением топливных фильтров ( в первый короткий период времени) сразу после того, как в загрязненую систему начнет поступать топливо с присадкой. [24]
Азот стоит несколько в стороне от доугих элементов V группы. Он представляет собой наиболее электроотрицательный элемент в этой группе, и, с нашей точки зрения, наибольшее значение имеют два следующие свойства азота. Для образования связи могут быть использованы только четыре орбиты L-оболочки, и поэтому азот образует не более четырех тетраэдрических связей, причем этот максимум достигается только в NHJ и в замещенных ионах аммония. В галогени-дах и в оксисоединениях образуются только три связи. Кроме того, так же как соседние элементы первого короткого периода - углерод и кислород, - азот характеризуется сильной тенденцией к образованию кратных связей. По этой причине азот образует значительное число соединений, которые не имеют аналогов у других членов этой группы; ввиду этого мы рассмотрим стереохимию азота отдельно. Таким образом, хотя азот и фосфор часто объединяют в одну группу, единственными соединениями этих элементов, которые структурно подобны друг другу, являются трехковалентные молекулы и ионы фосфония и аммония. Соединений азота, аналогичных пентагалогенидам фосфора, не существует, а между кислородными соединениями этих двух элементов, которые несколько потребнее будут рассмотрены ниже, имеется лишь небольшое сходство. Одноатомные ионы азота и фосфора встречаются только в твердом состоянии и только в солеподобных нитридах и фосфидах наиболее электроположительных элементов. [25]
Следует отметить целый ряд важных недостатков первоначальной теории. Во-иервых, она не дает объяснения величинам углов между связями, образуемыми элементом. Тетраэдрическое распределение четырех связей и октаэдрическое расположение шести связей было твердо установлено для ряда элементов путем изучения их классическими стереохимическими методами. Но как эти, так и другие, менее симметричные расположения связей, теоретически предсказать невозможно. Однако, если принять тетраэдряческое расположение четырех связей, образованных четырьмя парами электронов, составляющих устойчивый октет, как, например, в элементах двух первых коротких периодов, то пространственное распределение трех и двух связей согласуется с тем предположением, что неподеленные пары электронов ведут себя, как связи, занимая одно или два положения тетраэдрических связей. Так, NH - HOH имеет тетраэдрическую конфигурацию, тогда как молекула NH3 пирамидальна, причем неподеленная пара электронов занимает четвертое тетраэдрическое положение. [26]
Страницы: 1 2