Перхлорат - серебро
Cтраница 3
Это было приписано образованию соединения бензола с перхлоратом серебра, которое обычно считается стабильным до температуры 145 С. Он нашел, что хлорная кислота, использованная для приготовления этой соли, не содержала хлорида, хлората и органических соединений; примененный нитрат серебра содержал следы меди и железа, определяемые только спектроскопическим методом; комплекс эфир-перхлорат серебра не удалось обнаружить. Был сделан вывод, что взрыв вызван самим перхлоратом серебра. [31]
Аналогичный осадок получают при электролизе раствора сульфата или перхлората серебра, щелочных растворов нитрата серебра, содержащих гидроокиси аммония и калия. [32]
Реагент получают в нитрометане при 0 взаимодействием тозил-бромида с перхлоратом серебра. [33]
Ацетилен - очень слабая кислота, но с нитратом или перхлоратом серебра в соответствующей среде он образует карбид серебра и при этом выделяется кислота ( см. гл. [34]
Фишер [121] обнаружили, что в концентрированных водных растворах нитрата или перхлората серебра образуются растворимые комплексы ацетиленида и соли в молярном соотношении 1: 6, причем выделяющаяся минеральная кислота не разлагает эти комплексы и легко оттитровывается щелочью. [35]
Белые кристаллы состава C6He - AgC104 могут быть выделены из раствора перхлората серебра в бензоле. [36]
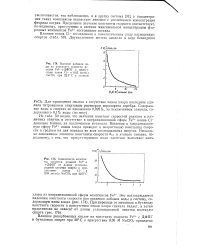 |
Зависимость константы скорости реакции Fe2 ДФПГ от длины углеводородной цепочки спирта в присутствии ионов С1 - и 0 05 моль / л NaClO4 при 22 5 С. [37] |
Для проведения опытов в отсутствие ионов хлора последние удаляли титрованием спиртовым раствором перхлората серебра. [38]
К раствору 4 г двухлористого трифенилвисмута в 50 мл ацетона прибавляют 3 25 г перхлората серебра в 10 мл сухого спирта. Выделившийся осадок хлористого серебра отделяют, фильтрат упаривают в вакууме при комнатной температуре до объема - 20 мл. На следующий день выделяется осадок, его отфильтровывают и промывают спиртом. Выход кристаллического вещества 1 504 г. Прибавлением к фильтрату 100 мл воды получают дополнительную порцию кристаллов. Для очистки перхлорат тетрафенилвисмутония дважды кристаллизуют из сухого этанола. [39]
Трихлорметилперхлорат был получен Биркенбахом и Губо65, а также Корренсом66 взаимодействием четыреххлористого углерода и перхлората серебра в присутствии небольшого количества хлористого водорода. При повторной дробной перегонке в вакууме в отсутствие влаги была получена бесцветная жидкость, которая затвердевала при - 55 С. [40]
В качестве окислителей применяют: йодноватую кислоту, дымящую серную кислоту, азотную кислоту и перхлорат серебра. В качестве веществ, связывающих иодистоводородную кислоту с образованием соли, применяют окись ртути, щелочи, калиевые соли слабых кислот и буру. Иод применяют главным образом в виде растворов в метиловом или этиловом спирте или в водном растворе йодистого калия. Для удаления избытка иода из реакционной смеси используют водный раствор йодистого калия, щелочь или ртуть. Органическое соединение, подлежащее иодированию, растворяют в эфире или бензоле и действуют смесью иода и перхлората серебра; последнее служит для связывания йодистого водорода. Этот метод дает хорошие результаты даже при низких температурах. Для связывания выделяющейся хлорной кислоты применяют карбонаты кальция или магния. По этому методу из толуола в темноте и при низкой температуре получают иодтолуол, на свету же иод вступает в боковую цепь. [41]
В качестве окислителей применяют: йодноватую кислоту, дымящую серную кислоту, азотную кислоту и перхлорат серебра. В качестве ве-шеств, связывающих иодистоводородную кислоту с образованием соли, применяют окись ртути, щелочи, калиевые соли слабых кислот и буру. Иод применяют главным образом в виде растворов в метиловом или этиловом спирте или в водном растворе йодистого калия. Для удаления избытка иода из реакционной смеси используют водный раствор йодистого калия, щелочь или ртуть. Органическое соединение, подлежащее иодированию, растворяют в эфире или бензоле и действуют смесью иода и перхлората серебра; последнее служит для связывания йодистого водорода. Этот метод дает хорошие результаты даже при низких температурах. Для связывания выделяющейся хлорной кислоты применяют карбонаты кальция или магния. По этому методу из толуола в темноте и при низкой температуре получают иод-толуол, на свету же иод вступает в боковую цепь. [42]
Реакцией ( 511) с бромистым бензилом и последующей обработкой синтезированной арсониевой соли спиртовым раствором перхлората серебра получен правовращающий перхлорат метил-н. Уменьшение величины оптического вращения связано, вероятно, с частичной рацемизацией () - бромистого метил-н. Восстановление ( Д1П) гексахлор-дисиланом протекает в мягких условиях с высоким оптическим выходом и почти полным сохранением конфигурации у атома мышьяка. [43]
Страницы: 1 2 3