Перхлорат - церие
Cтраница 1
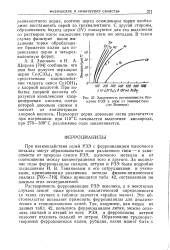 |
Зависимость растворимости бро. [1] |
Перхлорат церия довольно легко разлагается при нагревании: при 115 С начинается выделение кислорода, при 270 - 300 С разложение соли заканчивается. [2]
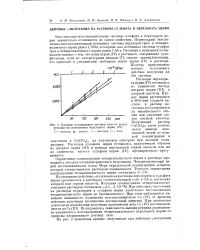 |
Влияние насыщающего раствор газа на выход реакции восстановления перхлората церия ( IV. О - водород. д-воздух. х - кислород. П - азот. [3] |
Растворы перхлората церия ( IV) готовились из химически чистых нитрата церия ( III) и хлорной кислоты. [4]
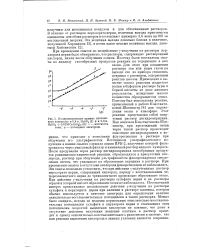 |
Поляризационные кривые платинового электрода вО 8н. H2S04 ( J и в 0 8н. H2S04 0 01М Се ( 804Ь ( 2. i - плотность тока. ф - потенциал электрода. [5] |
В отличие от растворов перхлората церия, величины выхода практически одинаковы для обоих растворов и составляют примерно 3 6 иона на 100 эв поглощенной энергии. [6]
Окислительно-восстановительные системы сульфата и перхлората церия значительно отличаются по своим свойствам. Нормальный окислительно-восстановительный потенциал системы перхлорат трех - и четырехвалентного церия равен 1 700 в, в то время как потенциал системы сульфат трех и четырехвалентного церия равен 1 48 в. Различие в величинах потенциалов связано с тем, что ионы церия ( IV) в растворах, содержащих сульфат-ионы, судя по литературным данным [7], сильно закомплексованы, что приводит к уменьшению свободных ионов церия ( IV) в растворе. [7]
Антраниловую кислоту можно также титровать раствором перхлората церия [837] или при малых количествах кобальта определять спектрофотометрически при 550 ммк с хлоргидра-том М - ( 1-нафтил) этилендиамина после диазотирования. [8]
Смит и Дьюк88 применяли в качестве окислителя раствор перхлората церия ( IV) в 4 М хлорной кислоте; авторы показали, что при комнатной температуре происходит стехиометри-ческое окисление целого ряда соединений. Как правило, вещества, содержащие активные метиленовые группы, и полиокси-соединения, содержащие гидроксильные группы у соседних углеродных атомов, окисляются до жирных кислот, кетонов, альдегидов ( но не до формальдегида) и двуокиси углерода. Исключение составляет глицерин - для его окисления необходимо нагревание при 45 С в течение 15 мин. Ацетон, ацеталь-дегид, а также соединения, образующие их при окислении, соприкасаясь с церием более 5 мин при 10 С, подвергаются заметному окислению, что приводит к ошибочным результатам. Формальдегид количественно окисляется до двуокиси углерода. В табл. 39 приведены примеры окисления ряда органических веществ, перечислены условия реакций и продукты окисления. [9]
При проведении опытов по воздействию - излучения на растворы перхлората церия было обнаружено, что растворы, содержащие растворенный кислород, пахли после облучения озоном. [10]
Специально поставленные опыты показали, что растворы сульфата и перхлората церия в присутствии платины достаточно устойчивы. [12]
Проведенное исследование действия у-излучения на окислительно-восстановительные системы: сульфат и перхлорат церия, бихромат калия и перманганат калия, имеющие высокий окислительный потенциал, показало, что при действии у-излучения происходит сдвиг окислительно-восстановительного равновесия в сторону образования восстановленных форм. Полученные результаты по зависимости выходов реакций восстановления от природы насыщающих раствор газов позволяют сделать вывод, что во всех изученных системах восстановление идет за счет Н - радикалов, образующихся в процессе радиолиза воды. [13]
Для окислительной деградации углеводов в последнее время весьма широко используется перхлорат церия. [14]
Примерно настолько же возрастает выход восстановления Се ( IV) в растворах перхлората церия при проведении процесса в присутствии платины. [15]
Страницы: 1 2