Петика
Cтраница 1
Петика показал, что адсорбция поверхностноактивных электролитов на поверхности раздела вода - воздух не может быть рассчитана по данным поверхностного натяжения при помощи уравнения Гиббса, за исключением тех случаев, когда в растворе присутствует избыток нейтрального электролита. В отсутствие нейтральной соли для оценки адсорбции из растворов простых ионо-генных ПАВ необходимо принять ряд допущений нетермодинамического характера. По данным межфазного натяжения он рассчитал поверхностный избыток по уравнению ( 108) в отсутствие нейтральной соли и показал, что вычисленные величины совпадают с экспериментальными значениями. [1]
По данным Петика [8], при использовании тщательно очищенного додецилсульфата натрия на кривых концентрационной зависимости поверхностного натяжения раствора этого ПАВ на границе с воздухом у / ( С) минимума не возникает. Двумя методами - измерения объема капель и уравновешивания пластинки ( по Вильгельми) - были получены идентичные значения поверхностного натяжения, причем равновесие в обоих случаях достигалось за 2 - 3 мин. [2]
Бейма и Петика [52] и приведенные там ссылки. Напомним рассмотренное в разд. [3]
По данным Петика [8], при использовании тщательно очищенного додецилсульфата натрия на кривых концентрационной зависимости поверхностного натяжения раствора этого ПАВ на границе с воздухом у / ( С) минимума не возникает. Двумя методами - измерения объема капель и уравновешивания пластинки ( по Вильгельми) - были получены идентичные значения поверхностного натяжения, причем равновесие в обоих случаях достигалось за 2 - 3 мин. [4]
Матиевич и Петика измерили поверхностные натяжения растворов октановой кислоты на 0 1 М iNaOH при 20 С и с помощью уравнения Гиббса рассчитали соответствующие я-0 - кривые для ионизованного монослоя. [5]
Поэтому Матиевич и Петика заключили, что уравнение ( 145) может быть справедливо и в отсутствие добавок соли, если растворы очень разбавлены, так что зависимость я - С линейна. [6]
Тэйлор, Хокки и Петика [84] получили данные по теплотам смачивания в воде поверхности образцов, которые предварительно прокаливали и затем регидратировали. [7]
Аналогичные результаты были бы применимы и для уравнения состояния БеЙма - Петика - Сазерленда ( разд. [8]
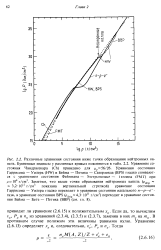
Заметим, что выше точки образования нейтронных капель ( pdri - - 3 2 - Ю1 г / см3 показана вертикальной стрелкой) уравнение состояния Гаррисона - Уилера гладко переходит в уравнение состояния идеального п-р - е - - газа, а уравнение состояния BPS G drip - 4 3 - 1011 г / см3) переходит в уравнение состояния Бейма - Бете - Петика ( ВВР) ( см. гл. [10]
Однако поверхностный потенциал на 1 М подложке значительно менее положителен, чем можно было ожидать, исходя из его значений для более разбавленных растворов. Петика и Фью [21 ] для монослоя октадецилсульфата на 1 М растворе хлорида натрия при площади 60 А2 на молекулу приводят значение поверхностного потенциала 5 - 10 мв. Таким образом, имеется довольно большое несоответствие между этой величиной и результатами Филлипса и Райдила, полученными для той же системы. Согласно Кокбейну, пленка додецилсульфата натрия, который хорошо растворим в воде, дает в сопоставимых условиях поверхностный потенциал примерно на 40 - 100 мв более отрицательный, чем пленка его нерастворимого С18 - аналога. [11]
Однако поверхностный потенциал на 1 М подложке значительно менее положителен, чем можно было ожидать, исходя из его значений для более разбавленных растворов. Петика и Фью [21 ] для монослоя октадецилсульфата на 1 М растворе хлорида натрия при площади 60 А2 на молекулу приводят значение поверхностного потенциала 5 - 10 мв. Таким образом, имеется довольно большое несоответствие между этой величиной и результатами Филлипса и Райдила, полученными для той же системы. Согласно Кокбейну, пленка додецилсульфата натрия, который хорошо растворим в воде, дает в сопоставимых условиях поверхностный потенциал примерно на 40 - 100 мв более отрицательный, чем пленка его нерастворимого С) 8-аналога. [12]
Петика и др. [9] подчеркивают, однако, что для микропористых адсорбентов удельные поверхности, определенные из теплот смачивания и изотерм адсорбции, могут быть совершенно различными. [13]
Отметим, что у нас все химические потенциалы включают массы покоя. В работе Бейма, Бете и Петика массы покоя нуклонов вычитаются из соответствующих выражений. [14]
Величина If и ее зависимость от А, конечно, должны влиять на результат. Если мы рассчитываем у на основании кривых давление - площадь по Бруку и Петика [18] ( теперь известно, что этот способ не корректен [17]), то получим т 65, используя 6Xц 2 25 А. [15]
Страницы: 1 2