Печень - свинья
Cтраница 2
Тот факт, что более чистые препараты каталагиг менее чувствительны к высоким температурам, чем экстракты, доказывается следующим опытом: каталаза из печени свиньи, предварительно очищенная троекратным осаждением спиртом, была растворена в воде и полученный раствор соответствующим разбавлением был доведен до той же степени активности, как и раствор крови. [16]
Из желчи других животных были выделены и другие желчные кислоты, как, например, оба изомера дезоксихолевой кислоты - гиоде-зоксихолевая кислота из печени свиньи и хенодезоксихолевая кислота из гусиной печени. Последняя содержится также в желчи человека. [17]
На первом этапе печень свиней временно подшивали к кровеносным сосудам людей, страдающих далеко зашедшей печеночной недостаточностью, подключая таким образом чужую печень как временный очистительный фильтр. [18]
Это отщепление аланина из боковой цепи оксикинуренина является необычной ферментативной реакцией, так как речь идет о не зависящем от кислорода расщеплении С-С - связи. Получением чистой кинурениназы из печени свиньи ( Висе и Вебер [53]) удалось доказать, что при этом расщеплении действует единственный фермент. Он содержит в качестве кофермента пиридоксальфосфат и осуществляет разрыв С-С - связи между J3 - иу-углеродными атомами боковой цепи гидролитическим путем. Кинурениназа отлична от ацилпирувазы, которая расщепляет 2 4-дикетожирные кислоты на жирную и пировиноградную кислоты, так как оба фермента можно препаративно отделить один от другого. [19]
На этой особенности было основано изучение ряда систем. Один из современных примеров такого исследования - проведенное Баркером и Дженксом [10] исследование эстеразы печени свиньи при нейтральных и кислых значениях рН ( фиг. [20]
Результаты, полученные из Канады, показывают присутствие ПХДД в пробах жировых тканей курицы, печени свиньи и ее жировых тканях; все из них были обследованы, поскольку они содержали более 70 нг / кг пентахлорфенола - консерванта дерева, но родственные соединения, содержащие меньше шести атомов хлора, обнаружены не были. [21]
Фермент из зародышей пшеницы был подвергнут 50-кратной очистке; показано, что для его действия обязательно присутствие аденозинтрифосфата и ионов магния и калия. Фермент катализирует также включение 535-цистеина в f - глутамилцистеин путем обмена в присутствии аденозинтрифосфата и ионов магния и калия. Сходный фермент получен из печени свиньи; для этой системы не требуется наличия ионов калия, однако ионы магния оказались необходимыми. Ферменты из зародышей пшеницы и из печени свиньи не идентичны ферменту, синтезирующему глутамин. В опытах с ферментом из зародышей пшеницы наблюдали обмен между неорганическим фосфатом и аденозинтрифос-фатом в присутствии глутамата, а также обмен фосфатной группой между АДФ и АТФ в отсутствие добавленных аминокислот. Интерпретация этих данных пока затруднительна. [22]
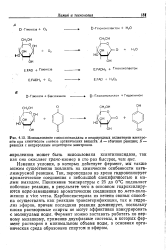 |
Использование глюкозооксидазы и неприродных акцепторов электро-ов при химическом синтезе органических веществ. А - обычная реакция. Б - реакция с неприродным акцептором электронов. [23] |
Изменяя условия, в которых действует фермент, мы также можем существенно повлиять на химические особенности катализируемой реакции. Так, пероксидаза из хрена гидроксилирует ароматические соединения с небольшой специфичностью и малым выходом. Понижение температуры с 25 до 0 С подавляет побочные реакции, в результате чего в основном гидроксилиру-ются / шра-замещенные ароматические соединения по мета-поло-жению и vice versa. Карбоксиэстераза из печени свиньи способна осуществлять как реакцию трансэтерификации, так и гидролиз эфиров, причем последняя реакция доминирует, поскольку плохо растворимые спирты не могут эффективно конкурировать; молекулами воды. Фермент можно заставить работать по первому механизму, применив двухфазные системы, в которых фермент растворен в минимальном объеме воды, а основная органическая среда образована спиртом и эфиром. [24]
Фермент из зародышей пшеницы был подвергнут 50-кратной очистке; показано, что для его действия обязательно присутствие аденозинтрифосфата и ионов магния и калия. Фермент катализирует также включение 535-цистеина в f - глутамилцистеин путем обмена в присутствии аденозинтрифосфата и ионов магния и калия. Сходный фермент получен из печени свиньи; для этой системы не требуется наличия ионов калия, однако ионы магния оказались необходимыми. Ферменты из зародышей пшеницы и из печени свиньи не идентичны ферменту, синтезирующему глутамин. В опытах с ферментом из зародышей пшеницы наблюдали обмен между неорганическим фосфатом и аденозинтрифос-фатом в присутствии глутамата, а также обмен фосфатной группой между АДФ и АТФ в отсутствие добавленных аминокислот. Интерпретация этих данных пока затруднительна. [25]
Страницы: 1 2