Пиридоксаминфосфат
Cтраница 2
Взаимопревращения а-амино - и а-кетокислот, связанные с циклом Кребса, осуществляются с участием трансаминиз. Трансаминазы, специфичные к аспарагиновой и глутаминовой кислотам, содержат в качестве простетической группы пиридоксальфосфат или пиридоксаминфосфат. Альдегид - м аминопроизводные способны к взаимопревращению. [16]
Первый этап реакции пореаминирования заключается в вытеснении е-амино-групны лизина аминогруппой соответствующей аминокислоты. Образующееся шиффово основание субстрата с пиридоксальфосфатом таутомеризуется; в результате гидролиза освобождается соответствующая кетокпслота и протеид пиридоксаминфосфата, к-рый, в случае аспартат - и аланин-аминотрансфераз, имеет независимо от рН максимум поглощения при 330 ммк. L-аспарагина и L-глутамииа на различные a - кетокислоты. [17]
Однако позднее было показано, что в данной системе активны оба кофермента [422]; в последующих работах найдено, что оба кофермента могут активировать и другие системы трансаминирования. Для максимального активирования фермента пиридоксаминофосфатом необходима более длительная предварительная инкубация, чем при применении пирид-оксальфосфата; это указывает на то, что аминная форма соединяется с белком фермента медленнее. Имеющиеся данные позволяют исключить возможность предварительного превращения пиридоксаминфосфата в пиридоксальфосфат в условиях данного эксперимента. Кофермент, очевидно, вступает с ферментом в прочную связь. [18]
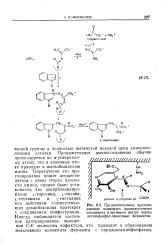 |
Предпочтительное протонирование нминового промежуточного соединения в активном центре пнрид-оксальфосфат-зависнмых ферментов. [19] |
Промежуточное иминосоединение обычно протонируется по а-углеродно-му атому, что в конечном итоге приводит к высвобождению амина. Теоретически это про-тонирование может осуществляться с обеих сторон плоскости имина, однако было установлено, что декарбокоилиро-вание L-тирозина, ь-лизина, L-глутамата и ь-гистидина под действием соответствующих декарбоксилаз протекает с сохранением конфигурации. Иногда наблюдается частичное протонирование положения С-4 молекулы кофактора, что приводит к образованию неактивного конъюгата фермента с пиридоксаминфосфатом. [20]
Аспартат-р-декарбоксилаза Cl, welchii отличается от других декарбоксилаз еще и тем, что она активируется не только пиридоксальфосфатом, но и очень малыми количествами а-кето-кислот. Это явление нельзя отнести за счет декарбоксилирова-ния щавелевоуксусной кислоты, возникающей в результате переаминирования между добавленной а-кетокислотой и acnapa - гиновой кислотой, поскольку а-аланин, образующийся при ферментативном карбоксилировании аспарагиновой кислоты в присутствии меченой пировиноградной кислоты, не содержит изотопной метки. По всей вероятности, активирующее действие добавленной а-кетокислоты связано с образованием пиридоксаль-фосфата в результате реакции переаминирования между а-кетокислотой и пиридоксаминфосфатом, присутствующим в ферментном препарате. [21]
Такие частично расщепленные препараты можно вновь активировать, добавляя пиридоксальфосфат или пиридоксаминфос-фат. При переаминировании аминокислота, которая служит субстратом, и фермент, связанный с пиридоксальфосфатом, конденсируются с образованием основания Шиффа. В результате последующих перемещений электронов происходит отщепление а-водородного атома и образуется таутомерное основание Шиффа, которое при гидролизе дает фермент, связанный с пиридоксаминфосфатом, и продукт реакции - кетокислоту. [22]
Аналогичные результаты были получены при исследовании процессов декарбоксилирования аминокислот. Позднее установили, что добавление пиридоксаля вместе с адено-зинтрифосфатом или же пиридоксальфосфата к клеткам S. Существуют убедительные данные, показывающие, что пирид-оксальфосфат участвует в декарбоксилировании аминокислот и что в трансаминировании могут принимать участие как пирид-оксальфосфат, так и пиридоксаминфосфат. [23]
Этот фермент, названный аланинрацемазой, был найден затем в клетках других микроорганизмов, в том числе у Leuconostoc mesenteroides, Escherichia coll, Bacillus subtllis и Pseudomonas fluorescens. Установлено, что добавление пирид-оксальфосфата значительно активирует очищенный фермент, тогда как пиридоксаминфосфат подобного действия не оказывает. Пировиноградная кислота в ходе реакции рацемизации не образуется. Скорость ферментативного превращения каждого из оптических изомеров аланина в рацемат одинакова. Фермент строго специфически катализирует реакцию рацемизации аланина; другие аминокислоты, например а-аминомасляная кислота, цистеин, серии, лейцин, треонин, пролин, оксипролин, лизин, аргинин, гистидин, тирозин, триптофан, аспарагиновая кислота и глутаминовая кислота, не подвергаются рацемизации. Участие витамина В6 в действии рацемазы послужило поводом к изучению неферментативных реакций рацемизации с участием пиридоксаля. Эти исследования привели к выводу, что механизм реакции рацемизации заключается в образовании шиффова основания из пиридоксаля и аминокислоты; при обратимых таутомерных превращениях этого промежуточного комплекса временно возникает двойная связь между а-углеродным атомом и азотом аминогруппы ( стр. [24]
Под трансаминированием ( переаминиро-ванием) подразумевают реакции межмолекулярного переноса аминогруппы от аминокислоты на а-кетокислоту без промежуточного образования аммиака. По меньшей мере 11 аминокислот способны вступать в реакции трансаминирования. Основными кетокислотами, принимающими участие в трансаминировании, являются пируват, ЩУК и а-кетоглутарат. Трансаминирование катализируют ферменты аминотрансферазы ( трансаминазы), которые содержатся в цитозоле и митохондриях клеток. В процессе катализа пиридоксальфосфат обратимо связывает аминогруппу, превращаясь в пиридоксаминфосфат. Схема реакции трансаминирования между глутаминовой кислотой и пируватом ( фермент - глутамат-пируват-аминотрансфераза или аланинаминотрансфераза, АлАТ): глутамат пируват - а-кетоглутарат аланин. [25]
Страницы: 1 2