Пирохлор
Cтраница 2
В структуре пирохлора ( разд. [16]
Абсолютное извлечение пирохлора в концентрат по схеме с термохимической подготовкой руды на 5 - 8 % выше, а извлечение апатита ( 55 %) - значительно выше, чем по другим схемам. [17]
Минералы лопарит, пирохлор, коппит и другие обладают невысокой химической прочностью и сравнительно легко разлагаются. Основная трудность - сложно отделить титан от ниобия и тантала. Ti, Та, Mb, присутствуя совместной оказывая друг на друга взаимное влияние, несколько теряют характерные индивидуальные свойства. [18]
Ввиду того что пирохлор и апатит при обработке карбонатных концентратов растворами хлористого аммония не подвергаются изменениям и высвобождаются из тонких сростков с карбонатами, изучалось дальнейшее механическое обогащение очищенных от карбонатов продуктов. Выявлено, что процессы концентрации пирохлора и апатита ( гравитация, флотация) из этих продуктов протекают успешно. [19]
К минералам типа пирохлора относится также минерал коп пит ( ниобат кальция, натрия и церия) и ряд других минералов. [20]
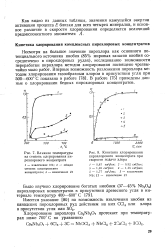 |
Влияние температуры на степень хлорирования пи-рохлорового концентрата.| Кинетика хлорирования пирохлорового концентрата при скорости подачи хлора. [21] |
Несмотря на большое значение пирохлора как основного потенциального источника ниобия ( 85 % мировых запасов ниобия сосредоточено в пирохлоровых рудах), исследованию возможности переработки пирохлора методом хлорирования посвящено чрезвычайно мало работ. В работе [75] приведены данные о хлорировании бедных пирохлоровых концентратов. [22]
Соединение Ег2Ш2О7 - типа пирохлора, рентгенографически не обнаружено. [23]
Структура построена по типу пирохлора со статистическим распределением одной седьмой части атомов кислорода. Она построена из двух типов полиэдров - октаэдров и кубов; вершина любого из полиэдров принадлежит еще одновременно трем соседним полиэдрам. Число кубов равно числу октаэдров. [24]
Несмотря на то, что пирохлоры известны уже давно, тщательный геометрический анализ из структуры до сих пор не проводился. Рассмотрим нормальные пирохлоры типа Aj Or. Как уже было сказано, у пирохлоров каждый катион типа В окружен шестью ионами кислорода. [25]
Оно имеет кристаллическую структуру типа пирохлора с кубической элементарной ячейкой, параметр которой равен 10 66 А. [26]
Твердая фаза этой стадии обработки пирохлора в основном рентгеноаморфна, но содержит немного сохранившегося пирохлора и образующейся новой кристаллической фазы. Результаты этих исследований позволили сделать вывод [41] о том, что при вымывании крупных катионов группы А кристаллическая решетка пирохлора деформируется с понижением сингонии, приближаясь к решетке Nb2O5, которая гидра-тируется в самом процессе сульфатизации и при обработке препаратов водными растворами. Такое представление вытекает из кристаллохимических особенностей пирохлора и других титано-танталониобатов. [27]
Он непостоянен, что объясняется изоморфизмом пирохлора и микролита. [28]
Это соединение имеет кристаллическую структуру типа пирохлора с кубической элементарной ячейкой РЬ2 ( Hfl Зз, Wo. [29]
Интересно отметить, что хотя анион дефицитных пирохлоров известно меньше, чем пирохлоров типа А Ог, среди первых найдено, по-видимому, несколько сегнетоэлектриков [ 21 и 24 ], в то время как среди последних найден только один сегнетоэлектрик. [30]
Страницы: 1 2 3 4