Плавление - нитрат
Cтраница 1
Плавление нитратов обычно протекает по типу диэлектрик-ионный расплав [19], в то время как природа химической связи в соединениях иодатов детально еще не изучена. [1]
Для точек плавления нитратов даются значения около 600 С, но примерно при таких же температурах начинается их термическое разложение. ЭО и окислы азота. Полный распад осуществляется только при довольно высоких температурах. По ряду Са-Sr - Ва термическая устойчивость нитратов несколько возрастает. [2]
Для точек плавления нитратов - даются значения около 600 С, но примерно при таких же температурах начинается их термическое разложение. Сначала они переходят в соответствующие нитриты и лишь при более сильном накаливании наступает разложение на ЭО и окислы азота. Полный распад осуществляется только при довольно высоких температурах. По ряду Са - Sr - Ва термическая устойчивость нитратов несколько возрастает. [3]
Низкая температура плавления нитратов, по-видимому, связана с добавочным вкладом в энтропию плавления, помимо конфигурационной энтропии. [4]
Выше точки плавления нитрата аммония, по данным [ 1о ], образуются азот и окись азота. [5]
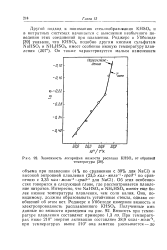 |
Зависимость логарифма вязкости расплава KHSO4 от обратной. [6] |
Об этих особенно стях говорится в следующей главе, где рассматривается плавление нитратов. Интересно, что NaHSO4 и NH4HSO4 имеют еще более низкие температуры плавления, чем соли калия. Они, по-видимому, должны образовывать устойчивые стекла, однако сообщений об этом нет. Вязкость при температуре плавления составляет примерно 1 3 пз. [7]
Механизм плавления нитратов металлов 1 - й группы. [8]
Расплавленные нитраты по сравнению с расплавленными га-логенидами обладают рядом особенностей. Так, температура плавления нитратов много ниже, энтропия плавления аномально велика, а изменение молярного объема, напротив, очень мало. [9]
Нитрат аммония очень хорошо растворим в воде. Так как температура плавления нитрата аммония сравнительно невысока, то при выпарке раствора NH4NO3 при температуре выше температур его кристаллизации вода может быть удалена практически почти полностью, причем раствор превратится в расплавленную соль. [10]
К 9 г нитрата натрия в стакане на 50 мл добавляют 10 мл 10 % - ной платинохлористоводородной кислоты. Смесь осторожно выпаривают досуха, не допуская плавления нитрата натрия. Полученную сухую соль всю сразу добавляют к 100 г предварительно нагретого в стакане емкостью 400 мл до 520 нитрата натрия, после чего нагрев прекращают. При смешении немедленно происходит выпадение осадка окисла, имеющего оливково-коричневый цвет. Массу охлаждают и нитрат натрия удаляют промыванием продукта примерно двумя литрами воды. Окись платины отделяют фильтрованием суспензии через бумажный фильтр на бюхнеровской воронке, тщательно промывают водой, не допуская подсыхания до завершения промывки. [11]
Все эти особенности ведут к усложнению модели расплавов. Дэвис с сотрудниками 84 ], уделившие этому вопросу особое внимание, предполагают, что при плавлении нитратов происходит ком-плексообразование. [12]
 |
Плавление хлоридов и нитратов. [13] |
Если допустить, что нитратные и сульфатные стекла состоят из таких же ионов, что и соответствующие кристаллы, то приходится рассматривать вопрос о том, почему другие ионные расплавы, например расплавы галогенидов щелочных и щелочноземельных металлов, не образуют столь же большого количества стекол. Многие авторы рассмотрели этот вопрос и пришли к единому мнению, что это объясняется различиями температур плавления. В табл. 30 показано, что температуры плавления нитратов Li, Na, К: Rb и Ag значительно ниже, чем у соответствующих хлоридов. Это сравнение имеет отношение к рассматриваемому вопросу, так как размеры ионов СГ и МОз - примерно одинаковы, а ионные радиусы равны 1 81 и 1 89 А соответственно. Подобная ситуация наблюдается и в двойных системах. Поскольку в нитратных и хлоридных системах прочность связей катион-анион примерно одинакова, отношение прочности связи к температуре ликвидуса в нитратных системах выше, и стеклообразование более вероятно. [14]
Титрованный раствор нитрата серебра можно приготовлять, точно отвешивая и растворяя требуемое количество препарата реактивной чистоты. Если препарат этот влажен, его предварительно измельчают в порошок и высушивают при 110 С. Последние следы влаги, порядка 0 1 - 0 2 %, остаются и при такой обработке. Плавление нитрата серебра следует проводить, защищая его от пыли и не поднимая температуру выше 250 С. [15]
Страницы: 1 2