Плавление - силикат
Cтраница 1
Плавление силикатов наступает позднее. Самые легкоплавкие из них становятся жидкими при температурах не ниже 1100 С, и надо учесть, что образование силикатов из окислов требует значительного перегрева, часто на 100 - 300 град. [1]
 |
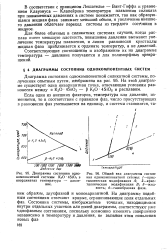
Вязкость силикатов и других неорганических веществ. [2] |
Высокая температура плавления силикатов и других оксидов, используемых в технологии неметаллических неорганических материалов самого разнообразного назначения, весьма осложняет исследование их строения в расплавленном состоянии. Эта причина сильно затруднила изучение расплавов силикатов по сравнению с другими жидкостями. Другим фактором, затрудняющим их изучение, является очень высокая вязкость, намного превышающая вязкость нормальных жидкостей, что обусловливает медленность достижения равновесия между расплавом и газовой фазой. Однако к настоящему времени о природе силикатных расплавов, их строении и свойствах накоплена значительная информация, позволившая сформулировать ряд обобщающих положений и гипотез. [3]
Определение температур плавления силикатов и окислов имеет весьма важное значение, так как большинство химических реакций в силикатных системах протекает достаточно интенсивно именно при очень высоких температурах. [4]
Способность плавня снижать температуру плавления силикатов используют для разложения почвы. [5]
Этим объясняются высокие температуры плавления силикатов и их нелетучесть. Это же приводит к свойственной некоторым силикатам способности легко обменивать ионы одних металлов на ионы других. Так, некоторые природные цеолиты или искусственно приготовляемые силикаты при взаимодействии с водными растворами солей могут частично обменивать содержащиеся в них катионы на катионы, имеющиеся в растворе. При этом обязательным условием является, чтобы размеры этих ионов не различались значительно. Так, ионы натрия Na ( радиус 1 05 А) легко обмениваются на ионы кальция Са2 ( радиус 0 95 А) в соотношении 2: 1, причем сохраняется нейтральность кристалла в целом. [6]
Этим объясняются высокие температуры плавления силикатов и их нелетучесть. Это же приводит к свойственной некоторым силикатам способности легко обменивать ионы одних металлов на ионы других. Так, некоторые природные цеолиты или искусственно приготовляемые силикаты при взаимодействии с водными растворами солей могут частично обменивать содержащиеся в них катионы на катионы, имеющиеся в растворе. При этом обязательным условием является, чтобы размеры этих ионов не различались значительно. Так, ионы натрия Na ( радиус 1 05 А) легко обмениваются на ионы кальция Са2 ( радиус 0 95 А) в соотношении 2: 1, причем сохраняется нейтральность кристалла в целом. Искусственные цеолиты используются также в качестве адсорбентов ( молекулярные сита, см. стр. [7]
Как известно, в большинстве случаев плавление силикатов характеризуется чрезвычайной замедленностью; тем же свойством обладают и процессы их полиморфных превращений. Поэтому применение флюсов бывает необходимым для исследования равновесий в силикатах; флюсы широко применяются в производстве огнеупорных тридимитовых кирпичей из кварцитов ( см. D. [8]
В этих системах изучен участок трехфазной кривой, исходящей из точки плавления силиката или окисла. Проекция этих кривых на плоскость р - t обращена выпуклостью к оси температур, что, по Бюхнеру [8], является характерным именно для сложного типа Р - Q-систем с расслаиванием. [9]
В соответствии с принципом Лешателье - Вант-Гоффа и уравнением Клаузиуса - Клапейрона температура плавления силиката при повышенных давлениях в системе понижается, так как образующаяся жидкая фаза занимает меньший объем, и увеличение внешнего давления облегчает переход системы из твердого состояния в жидкое. [11]
Небольшие отклонения от идеальных растворов у РЬО - SiO2 качественно подтверждаются невысокими температурами плавления силикатов свинца и отсутствием области расслаивания. [12]
Кремнефтористый натрий в жаростойком бетоне является не только ускерителем процесса твердения, но и плавнем, снижающим температуру плавления силиката. Поэтому нужно стремиться вводить не более 12 % кремнефтористого натрия от веса жидкого стекла. [13]
Сульфиды сплавляются между собой; однако капли их, разобщенные избытком углерода, трудно сливаются, также затруднено и плавление силикатов. Полурасплавленная шихта остается многофазной и сыпучей. [14]
Непосредственно измерить теплоту плавления или теплоту кристаллизации многих силикатов очень трудно, так как эти процессы протекают преимущественно при высоких температурах. Поэтому теплоту плавления силикатов определяют по методу растворения-их в плавиковой кислоте. Определяют ее для кристаллического и стекловидного состояний. Разность дает теплоту плавления данного вещества. Процесс растворения необходимо вести7 при одинаковых условиях. [15]
Страницы: 1 2 3