Гладкая платина
Cтраница 3
Скорость окисления муравьиной кислоты минимальна на гладкой платине; на платинированном пирографите и золоте удельная скорость окисления увеличивается с уменьшением количества катализатора на электродах. Как и в случае выделения водорода, это ускорение процесса мы связываем с активирующим влиянием катализатора на носитель. Только для муравьиной кислоты этот эффект выражен гораздо слабее, чем при выделении водорода. [32]
Величина емкости двойного слоя как на гладкой платине, так и на ртути и других гладких металлах лежит примерно в пределах от 10 до 40 мкф / см, она зависит от концентрации и состава электролита и потенциала в. Напротив, на платинированной платине при расчете на геометрическую поверхность получаются значения, увеличенные до 1000 раз. [33]
Измерительную цепь составляют из индикаторного электрода ( гладкая платина) и каломельного электрода сравнения. [34]
Электролитическое получение пероксобората осуществляют на анодах из гладкой платины при анодной плотности тока 4000 - - 6000 А / м2 и катодной плотности тока 1500 - 2000 А / м2, используя в качестве катодов Ст. Температуру в электролите поддерживают 10 - 12 С путем пропускания охлаждающей воды через электроды коробчатой формы. [35]
Такие же соотношения имеют место и для гладкой платины. [36]
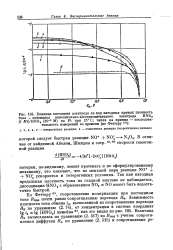 |
Влияние состояния электрода на ход катодных кривых плотность. [37] |
Так как катодная предельная плотность тока на гладкой платине не наблюдается, диссоциация HN02 с образованием N02 и N0 может быть недостаточно быстрой. [38]
Нам кажется, что электроды, покрытые гладкой платиной, могут найти себе применение в тех случаях, когда желательно избегнуть значительней адсорбции из растворов, которая может итти на платиновой черни, а также при измерении электропроводности is растворах, дающих плохой минимум. [39]
Каталитические свойства проявляют платиновая и палладиевая чернь, гладкая платина, палладий или иридий. [40]
Вместе с тем известно, что платинированная и гладкая платина отличаются по электродным свойствам. [41]
Каталитические свойства проявляют платиновая и палладиевая чернь, гладкая платина, палладий или иридий. [42]
В щелочном растворе обычно применяют аноды тоже из гладкой платины и окиси свинца, а кроме того, из железа и угля. [43]
При получении гшгогалогенитов реакциями замещения применяют электроды из гладкой платины в электролите со щелочной или щелочноземельной солью галоида. Галоид выделяется на аноде, а водород-на катоде. Галоид диффундирует от анода к катоду, встречает образующуюся на катоде щелочь и дает гипо-галогенит, который реагирует с органическим соединением. Если применяют галогениды калия или натрия, то раствор нужно держать нейтральным, добавляя углекислый газ или иод в случае йодистого электролита. Иод восстанавливается в иодистоводород-ную кислоту, которая нейтрализует щелочь. Другим методом является использование вспомогательного катода в пористом сосуде. При этом на главном катоде количество щелочи образуется неполное. [44]
Если взять два разных электрода: один из гладкой платины, , а другой из платины, покрытой платиновой чернью, то в силу сказанного ( если давление, под которым поглощается водород, одинаково) между этими электродами в одном и том же растворе окажется довольно значительная разность потенциалов Если же взять два совершенно одинаковых электрода, но насыщенных водородом при разных давлениях, и поместить их в один и тот же раствор, то и в этом случае также должна получиться разность потенциалов. [45]
Страницы: 1 2 3 4