Защитная оксидная пленка
Cтраница 3
Кобальт и никель устойчивы во влажном воздухе благодаря образованию защитной оксидной пленки. При нагревании железо, кобальт и никель взаимодействуют со многими окислителями. В атмосфере О2 железо сгорает до Fe2O3, кобальт и никель - до СоО и NiO. В мелкодисперсном состоянии эти металлы пирофор-ны - самовоспламеняются на воздухе. С серой металлы образуют моносульфиды FeS, CoS и NiS, которые хорошо растворимы в жидких металлах и способствуют образованию трещин при кристаллизации. Механические свойства сплавов на основе железа, кобальта и никеля при этом ухудшаются. [31]
При повышении анодного потенциала может быть достигнут потенциал пробоя защитной оксидной пленки на титане, после чего наступает быстрое разрушение титановой основы электрода. Потенциал пробоя зависит от состава электролита и температуры процесса. Обычно он значительно превышает анодный потенциал в производстве химических продуктов электрохимическим способом, но сильно снижается в концентрированных хлоратных или перхло-ратных растворах при низких концентрациях хлорида и повышенных температурах. Путем правильного выбора условий электролиза процессы получения хлора, хлоратов, перхлоратов, перекиси водорода и других продуктов можно проводить при потенциале анода ниже критического потенциала пробоя, что делает аноды на титановой основе пригодными для использования в перечисленных процессах. [32]
Алюминий обладает высокой коррозионной стойкостью вследствие образования на поверхности защитной оксидной пленки А Оз - Эта пленка затрудняет пайку алюминиевых проводов обычными методами. Необходим специальный припой или ультразвуковые паяльники. Места контакта алюминиевого провода с медным следует покрывать лаком для защиты от атмосферной коррозии. Во влажной атмосфере алюминий в контакте с медью быстро разрушается вследствие электрохимической коррозии. [33]
Водородные ионы повышают скорость коррозионных процессов и одновременно уменьшают прочность защитной оксидной пленки на поверхности металла. [34]
На практике антикоррозионные свойства меди в значительной степени определяются прочностью защитной оксидной пленки, замедляющей дальнейшее разрушение металла при воздействии коррозии. При нагревании свыше 180 С медь окисляется, и при температуре до 300 С оксидная пленка состоит почти исключительно из оксида меди СиО - вещества черного цвета, легко образующегося при накаливании меди на воздухе. [35]
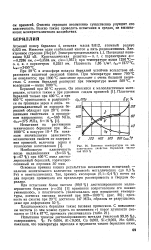 |
Влияние температуры на механические свойства бериллия чистотой 99 9 %. [36] |
При 20 С в атмосфере воздуха бериллий устойчив вследствие образования защитной оксидной пленки. При температуре выше 700 С он окисляется; при 1000 С окисление проходит с очень большой скоростью. С азотом бериллий реагирует при температуре выше 500 С, с водородом - выше 1000 С. [37]
Естественно, что создание условий, при которых происходит нарушение поверхностных защитных оксидных пленок, приводит к возможности проявления высокой химической активности титановых сплавов и к изменению в результате этого их прочности. К числу таких условий прежде всего относится малоцикловое нагружение в коррозионной среде, при котором нарушение защитной пленки в результате циклических деформаций может опережать скорость ее регенерации. Так как скорость регенерации пассивности существенно зависит от состава сплава, его термической обработки, состава и кислотности среды, условий развития трещины, влияние коррозионной среды на малоцикловую долговечность имеет разноплановый характер ( см. гл. При рассмотрении влияния коррозионной среды на малоцикловую долговечность прежде всего необходимо изучить особенности влияния скорости деформирования и наличия концентраторов напряжений. Исследованиями установлено следующее: для самопассивирующихся сплавов, к которым относятся и титановые, характерно, что максимальной чувствительности к коррозионной среде, переходу металла в активное состояние соответствует вполне определенный электрохимический потенциал. Изменение скорости деформации существенно влияет на величину потенциала. [39]
По отношению к воздуху и воде эти металлы устойчивы вследствие образования защитных оксидных пленок. Молибден и вольфрам устойчивы по отношению к разбавленным кислотам. По отношению к растворам щелочей в присутствии окислителей наиболее устойчив хром, менее стоек молибден и неустойчив вольфрам. [40]
Химическая активность их невелика, что обусловлено образованием на их поверхности защитных оксидных пленок. Цирконий и гафний устойчивы к действию растворов щелочен, азотной и хлороводородной кислот. [41]
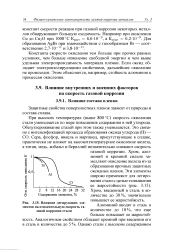 |
Влияние легирующих элементов на относительную скорость газовой коррозии стали. [42] |
Хром, алюминий и кремний сильно замедляют окисление железа из-за образования прочных защитных оксидных пленок. Хром, введенный в сталь в количестве до 30 %, значительно повышает ее жаростойкость. [43]
Дальнейшее повышение скорости воды может привести к интенсификации коррозионных процессов вследствие срыва защитных оксидных пленок. За счет усиления турбулентности потока при скоростях воды порядка 2 5 - 3 0 м / сек здесь часто наблюдается возникновение так называемой ударной коррозии. [44]
Очевидно, в этих условиях щелочность воды недостаточна для: поддерживания сохранности защитной оксидной пленки. Для протекания вышеуказанной реакции вовсе не требуется, чтобы котловая вода разлагалась с образованием газообразных водорода и кислорода; для протекания такого процесса требуется очень высокая температура, ибо даже при 650 С и 98 ати разложение пара дает все-то 0 01 мг / кг кислорода. Очевидно, в большинстве случаев имеет место прямое взаимодействие металла с водой. При температурах 480 - 540 С взаимодействие перегретого пара с металлом сопровождается образованием слоя окислов железа, прочно приставшего к внутренней поверхности пароперегревательных труб, изготовленных из малоуглеродистой стали. При более высоких температурах та же картина наблюдается для труб, изготовленных из легированных сталей. [45]
Страницы: 1 2 3 4