Плотность - жидкая вода
Cтраница 4
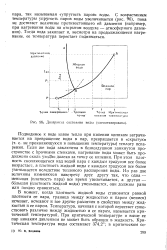 |
Диаграмма состояния воды ( схематизирована. [46] |
Если же вода заключена в безвоздушном замкнутом пространстве с прочными стенками, нагревание воды может быть продолжено сколь угодно далеко за точку ее кипения. При этом плотность скопляющегося над водой пара с каждым градусом все более возрастает, а плотность жидкой воды с каждым градусом все более уменьшается вследствие теплового расширения воды. Но раз две величины изменяются навстречу друг другу так, что одна - меньшая ( плотность пара) все время увеличивается, а другая - большая ( плотность жидкой воды) уменьшается, они должны рано или поздно сравняться. [47]
Авторами изучено влияние природы обменного катиона на адсорбционную емкость клиноптилолита и поведение молекул воды при его нагревании. Для исследования использовались катионные формы клиноптилолита месторождения Дзегви, декатионированный и деалюминированный клиноптилолитиз этого месторождения. Приблизительные значения внут-рикристаллического объема, занятого молекулами воды, вычислены из отношения н2о / Уц, где l / HjO - объем, занимаемый водой, содержащейся в 100 г цеолита ( принято, что плотность воды, находящейся в кристаллах цеолита, равна плотности жидкой воды); Уц - объем, занимаемый 100 г цеолита, вычисленный по данным о плотностях соответствующих образцов. Установлено, что с увеличением размера катионов количество цеолитной воды в клиноптилолите заметно уменьшается. Частичную дегидратацию клиноптилолита при замещении более мелких катионов на более крупные легко объяснить уменьшением свободного внутри-кристаллического объема. На кинетику дегидратации определенное влияние оказывает и катионная форма клиноптилолита. Уменьшение энергии активации Е дегидратации с возрастанием размеров катионов подтверждает представление о взаимодействии молекул воды с обменными катионами во внутрикристаллическом пространстве цеолитов. [48]
 |
Схематическое изображение структурных особенностей молекулы воды и водородной связи.| Структура жидкой воды в модели мерцающих кластеров Френка - Вина. [49] |
Для объяснения аномальных свойств воды в жидком состоянии учеными созданы различные модели ее структуры. Упорядоченное ( кристаллическое) расположение частиц воды в жидком состоянии доказано экспериментально. Полагают, что при плавлении льда его решетка частично разрушается и эти пустоты и ажурная структура льда заполняются освободившимися молекулами воды. Плотность жидкой воды вследствие этого увеличивается. Учеными подсчитано, что в жидкой фазе при 0 С несвязанные, заполняющие пустоты молекулы составляют около 16 % от их общего количества. [50]
Интересно, что такое расположение очень далеко от наиболее плотной укладки молекул. Это происходит потому, что при размещении молекул в более плотной структуре не могла бы сохраниться такая их взаимная ориентация, которая отвечает тетра-эдрическому распределению четырех связей кислородного атома и которая необходима для возникновения водородной связи. Искажение же валентных углов требует затраты значительного количества энергии. Всем этим объясняется рыхлая структура льда и тот факт, что плотность льда меньше, чем плотность жидкой воды. В состав ионных кристаллов могут входить и некоторые нейтральные молекулы, достаточно малые по размеру и обладающие значительной полярностью или способностью к образованию донорно-акцепторной связи или водородной связи. Это относится главным образом к молекулам воды и в меньшей степени к молекулам аммиака. [51]
Интересно, что такое расположение очень далеко от наиболее плотной укладки молекул. Это происходит потому, что при раз мещении молекул в более плотной структуре не могла бы сохра киться такая их взаимная ориентация, которая отвечает тетраэд-рическому распределению четырех связей кислородного атома и-которая необходима для возникновения водородной связи. Искажение же валентных углов требует затраты значительного количества энергии. Всем этим объясняется рыхлая структура льда и тот факт, что плотность льда меньше, чем плотность жидкой воды. [52]
Интересно, что такое расположение очень далеко от наиболее плотной укладки молекул. Это происходит потому, что при размещении молекул в более плотной структуре не могла бы сохраниться такая их взаимная ориентация, которая отвечает тетраэд-рическому распределению четырех связей кислородного атома и которая необходима для возникновения водородной связи. Искажение же валентных углов требует затраты значительного количества энергии. Всем этим объясняется рыхлая структура льда и тот факт, что плотность льда меньше, чем плотность жидкой воды. [53]
Страницы: 1 2 3 4