Плотность - упаковка - молекула
Cтраница 1
Плотность упаковки молекул, Одним из важнейших принципов кристаллохимии является принцип плотнейшей упаковки, согласно которому наиболее вероятной и, следовательно, наиболее устойчивой структуре соответствует плотная укладка ионов, атомов или молекул в кристалле. Тогда остается наименьшее по объему свободное пространство между этими частицами. Как и пизкомолеку-лярные органические вещества, полимеры подчиняются принципу плотной упаковки, и в кристаллической решетке макромолекулы должны быть уложены как можно плотнее. Существует несколько возможностей образования плотной упаковки полимерных цепей. [1]
Плотность упаковки молекул в структуре молекулярного кристалла характеризуется коэффициентом упаковки k, который представляет собой частное отделения объема молекулы, вычисленного по величине межмолекулярного радиуса, на объем той же молекулы, установленный по данным рентгеновских измерений. Значения коэффициента упаковки для молекулярных кристаллов находятся в пределах от 0 65 до 0 77, как и для плотных укладок эллипсоидов и шаров. Вещества, имеющие молекулы такой формы, что любая их укладка не может иметь коэффициент упаковки больше 0 6, при отвердевании образуют не молекулярные кристаллы, а стекла. [2]
Однако плотность упаковки молекул раствора и фактор неидеальности d не изменяются симбатно. При переходе от растворов кислот в н-гептане до растворов в СС14 и бензоле отклонение от свойств идеальных растворов повышается, a dE проходит через минимум. Следовательно, в растворе бензола происходит не только диссоциация комплексов молекул кислота - кислота, но и образование л-комплексов между молекулой кислоты и бензола. Обе характеристики - фактор d и dE - взаимно дополняют информацию о реорганизации структуры жидких систем при образовании растворов. В малоактивных растворителях фактор d меняется в результате диссоциации комплексов, состоящих из однотипных молекул, а в растворе более активных растворителей - благодаря взаимодействию молекул разных типов. [4]
 |
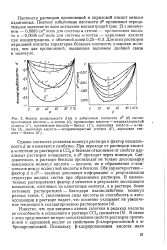
Зависимость молекулярных площадей от константы СБЭТ для азота, аргона и криптона. [5] |
Как указывалось, плотность упаковки молекул зависит в первую очередь от энергии адсорбции и величины оот антибатны этой энергии. Некоторое представление об этой зависимости можно получить из сопоставления значений ит энергетической константой С вэт как это было сделано впервые Киселевым ж Эльтековым [9] для w - пентана. На рис. 7 представлена зависимость чт-от СБЭТ для изученных трех адсорбатов. Конечно, приведенные кривые дают лишь качественное представление об этой зависимости. Весьма желательно прямое сопоставление от-с величинами калориметрически определенных теплот. В [ 101 высказана идея о зависимости ит от степени локализации адсорбированных молекул, которая, в свою очередь, также должна зависеть от энергии адсорбции. [6]
 |
Схемы строения полимера.| Структура полимера в твердом состоянии. [7] |
В кристаллическом состоянии плотность упаковки молекул осуществляется за счет параллельного расположения их осей. [8]
 |
Тетраэдриче-ская структура кристаллической решетки льда. [9] |
В жидком состоянии плотность упаковки молекул воды весьма велика. Поэтому вероятность ассоциации молекул возрастает. Так как плотность жидкой воды мало зависит от давления, вероятность ассоциации молекул зависит только от температуры. [10]
Рассмотрим теперь влияние плотности упаковки молекул твердого тела в поверхностном слое. В других случаях большую роль играют и другие факторы - плотность полимера, строение адсорбционной пленки. [11]
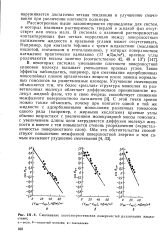 |
Смачивание низкоэнергетических поверхностей различными жидкостями. а - вода. б - йодистый метилен. в-гексадекан. [12] |
В некоторых системах уменьшение плотности поверхностной упаковки молекул вызывает уменьшение краевых углов. [13]
Температура плавления вещества зависит от плотности упаковки молекул; например, н-парафины с относительно регулярной плотной упаковкой изотактических углеродных цепей характеризуются более высокой температурой плавления, чем изомерные им парафины с разветвленной углеродной цепочкой. Поскольку в ГЖХ целесообразно применять неподвижные фазы с минимальным НТП, стараются в качестве неподвижных фаз использовать соединения, углеродные цепочки молекул которых содержат большое число разветвлений. Наличие в молекуле атомных групп, вступающих в электростатическое или специфическое взаимодействие, повышает температуру плавления вещества. Особенно высокие значения температур плавления наблюдаются для соединений, молекулы которых содержат большое число гидроксильных групп. [14]
 |
Схема сорбционной установки. [15] |
Страницы: 1 2 3 4