Повышенная электронная плотность
Cтраница 1
Повышенная электронная плотность на этом атоме азота должна отражаться благоприятно на процессе расщепления. [1]
Повышенная электронная плотность в положениях 1 и 3 проявляется реакциями ароматического замещения ( реакцией Фриделя-Крафтса с уксусным ангидридом и хлорным оловом и реакцией нитрования), протекающими в этих положениях. Однако эти реакции трудно осуществить вследствие значительной склонности азулена превращаться под влиянием кислых реагентов в аморфные полимеры. [2]
Повышенная электронная плотность на атомах углерода приво дит к тому, что эти гетероциклические соединения легко вступают в реакции электрофильного замещения. [3]
Наличие повышенных электронных плотностей в op / no - и пара-положениях к метальной группе приводит к образованию пара - и opmo - толуолсульфокислот. [4]
Наличие повышенных электронных плотностей в орто - и пара-положениях к метильнои группе приводит к образованию пара - и opmo - толуолсульфокислот. [5]
Вследствие повышенной электронной плотности в кольце / электронов приходятся на пять атомов) пиррол, фуран и тиоф называют л-избыточными системами. [6]
Благодаря повышенной электронной плотности молекулы фенола в орто - и пара-положениях по сравнению с бензолом или метилбензолами, реакция передачи ( диспропорционирования) метильных групп от полиметилбензолов к фенолу должна протекать с большей скоростью, чем аналогичные реакции в системе полиметилбензол - бензол и с меньшей степенью превращения, чем в системе полиметилфенол - фенол. [7]
Реакции способствует повышенная электронная плотность в ароматическом ядре. [8]
Мономеры с повышенной электронной плотностью ( стирол, аллиловый спирт) при термическом воздействии не реагируют с каучуком. [9]
Для индола характерна повышенная электронная плотность в положении 3, вследствие чего он способен участвовать в реакциях в таутомерией форме индоленина ( 19), которая в свободном состоянии не существует. [10]
Аналогичные данные о повышенной электронной плотности по направлениям от центрального атома к атомам, находящимся в углах тетраэдра решетки алмаза, рассматриваются в работе [136] как прямое доказательство существования в кристалле алмаза тетраэдрически направленных ковалентных связей. [11]
Двойная связь имеет повышенную электронную плотность, поэтому она легко присоединяет электрофильные ( любящие электроны) частицы. [12]
Нуклеофильные реагенты характеризуются повышенной электронной плотностью. Различают несколько типов таких реагентов, среди которых существенную роль играют анионы, содержащие гетероатомы. [13]
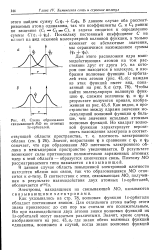 |
Схема образования. [14] |
В данном случае область повышенной электронной плотности находится вблизи оси связи, так что образовавшаяся МО относится к о-типу. [15]
Страницы: 1 2 3 4