Пятивалентный плутоний
Cтраница 2
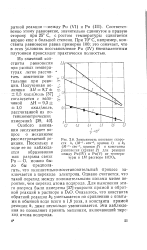 |
Зависимость констант скорости kl ( М-1 сек-1, кривая / и k2 ( М -. сект1, кривая 3 и константы равновесия ( кривая 2 для реакции между Pu ( IV и Pu ( V от температуры в 1М растворе НС10. [16] |
Соответственно этому равновесие, значительно сдвинутое в правую сторону при 25 С, с ростом температуры сдвигается вправо еще в большей степени. При 70 С, например, константа равновесия равна примерно 100; это означает, что в этих условиях восстановление Ри ( IV) пятивалентным плутонием происходит практически полностью. [17]
Кинетическое исследование радиационного окисления мышьяковистой кислоты привело в выводу [2], что неустойчивые соединения четырехвалентного мышьяка ( As02 или H2AsOs) играют существенную роль в этой реакции, хотя такие соединения не известны в устойчивом виде. Интересно было установить, какую роль играют в радиационном окислении четырехвалентного урана известные, но неустойчивые соединения Uv ( UO 2) и сравнить ее с возможной ролью пятивалентного плутония при радиационном восстановлении соединений. [18]
Диспропорционирование ускоряется в ком-плексообразующих растворах, особенно в сернокислых. При рН 3 5 в солянокислых и азотнокислых растворах концентрация пятивалентного плутония не изменяется в течение нескольких дней. При рН 1 и рН 7 идет быстрое диспро-порционирование. Стабильность пятивалентного плутония уменьшается с увеличением температуры, причем растворы с большими концентрациями плутония более чувствительны к ее изменению. [19]
Нептуний занимает особое место среди актиноидов по устойчивости его пятивалентного состояния в водных растворах. Установлено образование оксалатных комплексов, но относительно комплексообразования между ионами пятивалентного плутония и нитратом, хлоридом и сульфатом опубликовано еще мало работ. Пятивалентный нептуний легко окисляется в нептунил такими окислителями, как четырехвалентный церий и бромат-ион. Как правило, растворы шестивалентного нептуния устойчивы. Комплексные ионы шестивалентного нептуния должны напоминать комплексные ионы шестивалентного плутония, но для подтверждения этого еще не имеется достаточных экспериментальных данных. [20]
Весьма интересен метод приготовления Pu ( V), предложенный Маркиным и Мак-Кеем [536] и основанный на быстром установлении равновесия между ионами плутония по реакции ( 22) ( стр. Равные объемы растворов Pu ( VI) и Pu ( III) в 0 2 М HNO3 с концентрацией каждого компонента 2 мг / мл смешивают в присутствии 0 1 % - ного раствора дибутилфосфата в бензоле. Образующийся в процессе реакции между Pu ( VI) и Pu ( III) четырехвалентный плутоний экстрагируется в органическую фазу, а пятивалентный плутоний остается в водном слое. Pu ( VI) и Pu ( III) полностью превращаются в Pu ( IV) и Pu ( V) благодаря выводу Pu ( IV) из системы. [21]
Плутоний в соединениях может быть, подобно урану, трех -, четырех -, пяти - и шестивалентным, но, в отличие от урана, максимум устойчивости соединений сдвинут к низшим степеням окисления. В водных растворах наиболее устойчивы соединения четырехвалентного плутония; восстановлением их можно получить соединения трехвалентного плутония. При помощи окислителей легко могут быть получены соединения шестивалентного плутония. Растворы соединений пятивалентного плутония малоустойчивы. [22]
Диспропорционирование ускоряется в ком-плексообразующих растворах, особенно в сернокислых. При рН 3 5 в солянокислых и азотнокислых растворах концентрация пятивалентного плутония не изменяется в течение нескольких дней. При рН 1 и рН 7 идет быстрое диспро-порционирование. Стабильность пятивалентного плутония уменьшается с увеличением температуры, причем растворы с большими концентрациями плутония более чувствительны к ее изменению. [23]
Страницы: 1 2