Бромид - радий
Cтраница 1
Бромид радия, RaBr2 - 2H20, выделяется из водного раствора, полученного растворением карбоната радия в бромистоводородной кислоте. Бесцветные моноклинные кристаллы этого гидрата растворимы в воде и спирте. [1]
Хлорид и бромид радия исследованы в большей степени, чем другие известные соединения радия. [2]
Чтобы получить источник нейтронов, достаточно смешать бромид радия с порошком бериллия. [3]
 |
Характеристики нейтронных источников. [4] |
Радий-бериллиевые нейтронные источники представляют собой прессованную смесь бромида радия с порошкообразным бериллием, заключенную в двойную латунную оболочку цилиндрической формы. [5]
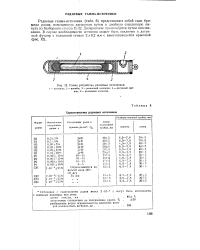 |
Схема устройства радиевых источников. 1 - источник. 2 - пломба. 3 - резиновый коллачек. 4 - латунный футляр. 5 - резиновый колпачек. [6] |
Радиевые гамма-источники ( табл. 6) представляют собой соль бромида радия, помещенную насыпным путем в двойную стеклянную ампулу из безборного стекла Ц-32. Дозирование производится путем взвешивания. [7]
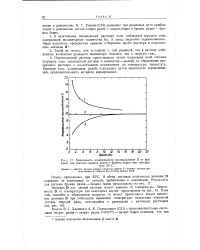 |
Зависимость коэффициента распределения D от времени для системы бромид радия - бромид бария при температуре 35 С. [8] |
С 15 ] указывает три различных пути приближения к равновесию систем хлорид радия - хлорид бария и бромид радия - бромид бария. [9]
Есяйьнам не удалось увидеть спектр эманации, то зато мы, к нашему изумлению, нашли в таких трубках ( с бромидом радия. Это был первый зарегистрированный случай превращения одного элемента в другой. [10]
Безводный бромид радия может быть получен растворением карбоната радия в НВг или многократной обработкой хлорида радия бромистоводородной кислотой с последующим упариванием и высушиванием при 120 - 150 С. Кристаллы дигид-рата бромида радия принадлежат к моноклинной сингонии и изоморфны с дигидратом бромида бария. [11]
Все вышеизложенное дает основание считать, что наблюдавшееся саморазложение сульфата радия идет преимущественно на поверхности и, таким образом, является вторичным, связанным с окружающей средой, процессом, который в воздухе и в воде может идти практически одинаковым образом. Это предположение подтверждается наблюдением над кристаллами бромида радия, которые после стояния на воздухе окрасились в коричневый цвет; если же незначительной добавкой воды растворить поверхностный слой, то окрашивание исчезает и кристаллы снова становятся белыми. [12]
Соли радия сами по себе тоже бесцветны. Однако некоторые из них, например хлорид и бромид радия, постепенно окрашиваются под действием излучения содержащегося в них радия и, наконец, приобретают окраску от коричневой до черной. При перекристаллизации они вновь становятся белыми. [13]
Соли радия сами по себе тоже бесцветны. Однако некоторые из них, например хлорид и бромид радия, постепенно окрашиваются под действием излучения содержащегося-в них радия и, наконец, приобретают окраску от коричневой до черной. При перекристаллизации они вновь становятся белыми. [14]
Источником получения радона являются радий и его соединения. Наилучшей эманирующей способностью обладают гидроокись, хлорид и бромид радия; сульфат радия - самое слабоэманирующее соединение радия. Радон полностью выделяется из солей радия при их плавлении. Обычно радон выделяется из подкисленных растворов ( рН 2 - - 2 5) хлористого или бромистого радия. [15]
Страницы: 1 2