Поведение - железо
Cтраница 2
Бросается в глаза различие в поведении железа и палладия, имеющих приблизительно одно и то же перенапряжение кислорода, при окислении нитрита, а также различие в выхо-дах по току при окислении нитрита на платиновом и иридиевом анодах. [16]
Другим примером неожиданного сопротивления окислению служит поведение железа в концентрированной серной кислоте. В этом случае на поверхности железа образуется пленка так называемого пассивированного железа ( по-видимому, тонкий слой Fe3O4), которая предотвращает дальнейшее воздействие кислоты на металл. Концентрированную серную кислоту редко хранят в больших количествах в железных или стальных емкостях. Такие емкости необходимо держать герметично закрытыми, так как влага, содержащаяся в воздухе, может разбавить кислоту настолько, что она будет способна взаимодействовать с железом. [17]
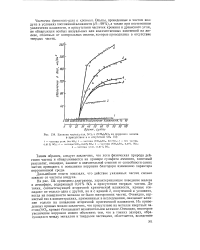 |
Влияние частиц угля, БЮг и ( NHUbSCU на коррозию железа в присутствии и в отсутствие 50г. [18] |
На рис. 134 приведены диаграммы, характеризующие поведение железа в атмосфере, содержащей 0 01 % БОг в присутствии твердых частиц. До точки, соответствующей вторичной критической влажности, кривые совпадают не только одна с другой, но и с кривой 3, полученной в условиях, когда на поверхности металла не было посторонних частиц. Очевидно, сернистый газ в концентрациях, примененных в исследовании, оказывает влияние только на появление вторичной критической влажности. Из приведенных кривых можно заключить, что присутствие на металле инертных частиц ( Si02, кривая 4) оказывает незначительное влияние. [19]
В первом обзоре обобщены данные, относящиеся к коррозионно-электро-химическому поведению железа, хрома, никеля, а также сплавов железо-хром, железо-никель, хром-никель, железо-хром-никель в кислых и в нейтральных растворах. [20]
Изучение условий соосаждения галлия с фосфатом кальция, а также поведения железа и алюминия в этих условиях ( рис. 3) позволило использовать эти данные для выделения галлия из бокситов ( см. стр. [22]
Электрохимическое поведение никеля в активном состоянии во многом сходно с поведением железа. В тех же условиях галогенид-ионы, присутствующие даже в небольших количествах, тормозят процесс, что можно связать с адсорбционным вытеснением ими ионов ОН 1 [ 36J, Скорость. [23]
Природа этих трех стадий связывания серы самым различным образом влияет на поведение железа в процессе обработки его соляной кислотой. Только химическая адсорбция оказывает каталитическое действие на коррозию железа. [24]
Такую защиту обычно называют пассивацией на основании наблюдений Фарадея над особенностями поведения железа. Когда металл реагирует с водой, он может либо образовывать растворимые катионы, либо непосредственно формировать пассивную пленку. [25]
Электрохимическое поведение железа, находящегося в зазоре, в растворах ортофосфата аналогично поведению железа в растворах нитрита натрия и чугуна в растворах бихромата калия. Потенциалы железа в узких зазорах с течением времени становятся более отрицательными и приобретают значения, равные - 0 5 В. [27]
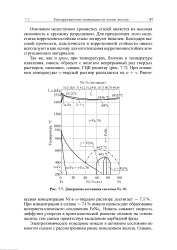 |
Диаграмма состояния системы Fe - Ni. [28] |
Электрохимическое поведение никеля в активном состоянии во многом сходно с рассмотренным ранее поведением железа. [29]
Показано, что поведение кобальта при соосаждении с фосфатом кальция резко отличается от поведения железа в этих условиях. [30]
Страницы: 1 2 3 4