Поведение - электрод
Cтраница 3
Поведение электрона а ящике не очень отличается от поведения электродов в реальных молекулах; в лч. СЭМО дает в приближенном выражении идею об энергиях спектроскопических перекодов; сейчас мы увидим, что ее можно использовать для оценки интенсивности. [31]
Поскольку анодные и катодные поляризационные кривые различны и поведение электродов неизвестно, при моделировании устанавливают нелинейные двухполюсники, соответствующие как анодному, так и катодному направлениям тока через каждый электрод. Каждый такой элемент включен последовательно с диодом, в результате чего в схеме автоматически устанавливается ток необходимой величины и направления. [32]
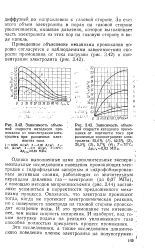
Однако выполненные нами дополнительные экспери -, ментальные исследования поведения промокающих электродов с гидрофильным запорным и 1идрофобизирован - ным активным слоями, работающих со значительным перепадом давления газ - электролит ( до 0 07 МПа), с помощью методов михрокиносъемки ( рис. 3.44) заставляют усомниться в корректности предложенного механизма процесса. Оказалось, что электроды промокают тогда, когда не протекает электрохимическая реакция, но с поверхности электрода на газовой стороне происходит испарение воды. И это промокание тем интенсив - г нее, чем выше скорость испарения. И наоборот, под то - ком нагрузки подача на реакцию увлажненного газа способна полностью прекратить процесс промокания. [34]
Проведенные нами исследования показали, что система процессов, определяющих поведение электродов в растворах метанола, несколько проще, чем система процессов в растворах более высоких спиртов и альдегидов. Поэтому изложение экспериментального материала и его обсуждение разделено на две части. В первую очередь будут рассмотрены данные по метанолу. [35]
 |
Определение общего потенциала фобщ четырехэлектродной системы путем сложения токов, прохп-дящих через электроды при заданном потенциале. [36] |
По теории многоэлектродных систем, разработанной Г. В. Акимовым и Н. Д. То-машавым, поведение электродов с промежуточными значениями потенциалов определяется то отношению их начальных потенциалов к общему, приобретаемому всей системой. Нахождение общего потенциала сложной системы сводится к построению суммарной поляризационной кривой в координатах потенциал-сила тока по известным поляризационным характеристикам, соотношению поверхностей и омическим сопротивлением в цепи каждого электрода. [37]
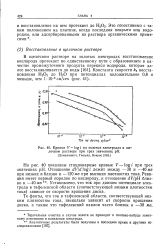 |
Кривые V - logi на золотых электродах в щелочном растворе при трех значениях рН. ( Дамьянович, Геншау, Бокрис. [38] |
Тщательная очистка в случае золота не приводит к сколько-нибудь заметному изменению в поведении электрода. [39]
С 1962 г. на кафедре электрохимии химического факультета МГУ проводятся работы по изучению поведения электродов из металлов платиновой группы в растворах предельных спиртов, альдегидов и кислот. [40]
 |
Конструкция твердого мембранного селек-трода. [41] |
Таким образом, приведенные значения являются лишь приблизительными и могут служить для общей оценки поведения электродов в различных растворах при концентрациях, используемых в измерениях. [42]
Этот метод открывает широкие возможности для исследования механизма питтинговой коррозии и установления общих закономерностей поведения сложного электрода. [43]
При выборе электродных материалов для осуществления электрохимического процесса необходимо обращать особое внимание на важность изучения поведения электродов в разбавленных водных растворах, какими являются большинство сточных вод. При исследовании этого вопроса возникает задача разработки более совершенных методик снятия поляризационных кривых в динамических условиях протекания процесса с изменяющимися физико-химическими свойствами растворов, которые оказывают влияние на изменение констант диффузий и скоростей электродных реакций. [44]
Сравнивая изменение электродных потенциалов в ходе разряда при первом и втором циклах, делают заключение о поведении электродов при хранении и о влиянии того или другого электрода на снижение емкости аккумулятора. [45]
Страницы: 1 2 3 4