Поведение - стеклянный электрод
Cтраница 1
Поведение стеклянного электрода в неводных щелочных растворах были объяснены на основании представлений о том, что возникновение отклонений при более низких значениях рН является результатом увеличения констант обмена стекла вследствие изменения соотношения в активности ионов водорода и катионов в различных неводных средах. [1]
Поведение стеклянного электрода в кислой и щелочной области, таким образом, объяснены нами на основе одних и тех же представлений. [2]
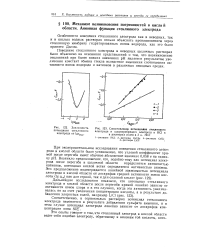 |
Сопоставление потенциалов стеклянного. [3] |
Поведение стеклянного электрода в неводных щелочных растворах было объяснено на основании представлений о том, что возникновение отклонений при более низких значениях рН является результатом увеличения констант обмена стекла вследствие изменения соотношения активности ионов водорода и катионов в различных неводных средах. [4]
Особенности поведения стеклянного электрода как в неводных, так и в кислых водных растворах нельзя объяснить проникновением через стеклянную мембрану гидратированных ионов водорода, как это было принято Долом. [5]
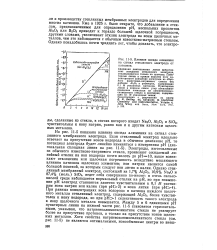 |
Влияние оксида алюминия на сигнал стеклянного электрода от катионов. [6] |
Сплошная диагональная линия представляет поведение стеклянного электрода, откликающегося только на протоны. Пунктирные линии в правом верхнем углу характеризуют поведение электрода из обычного известково-натриевого стекла без добавок AljOs в растворах, содержащих 0 1 М указанных катионов. Пунктирные линии в нижнем левом углу показывают поведение электрода из натриевоалюмо-силикатного стекла в растворах, содержащих 0 1 М указанных ионов. [7]
Таким образом, особенности поведения стеклянного электрода в неводных растворах щелочей объясняются разным соотношением активностей ионов водорода и натрия в воде и в неводных растворах. [8]
Таким образом, особенности поведения стеклянного электрода в неводных растворах щелочей объясняются разным соотношением в активностях ионов водорода и натрия в воде и в неводных растворах. [9]
Было проведено непосредственное экспериментальное сравнение поведения стеклянных электродов с водородным и амальгамным натриевым электродами. Исследованию были подвергнуты как рН - метрические стеклянные электроды типа Корнинг 015, так и электроды из стекла типа Иена 591П, а также электроды из стекол с широкой областью перехода водородной функции к натриевой. [10]
Было проведено непосредственное экспериментальное сравнение поведения стеклянных электродов с водородным и амальгамным натриевым электродами. Исследованию были подвергнуты как рН - метрические стеклянные электроды типа Корнинг 015, так и электроды из стекла типа Иена 59Ш, а также электроды из стекол с широкой областью перехода водородной функции к натриевой. [11]
В настоящее время кроме ионообменных теорий поведение стеклянных электродов объяснено на основе жидкостно-мембранной концепции, предусматривающей наличие в стекле анионных узлов - вакансий в качестве дискретных лигандов для переноса катионов. [12]
Отсюда очевидна важность теоретического обоснования уравнений, описывающих поведение стеклянных электродов в смешанных растворах, которые составляют эту систему и закладываются в программу счетно-решающего устройства. В упомянутых работах используются уравнения типа уравнений простой теории Б. П. Никольского для двух ионов [ уравнение ( 9) ( стр. [13]
Отсюда очевидна важность теоретического обоснования уравнений, описывающих поведение стеклянных электродов в смешанных растворах, которые составляют эту систему и закладываются в программу счетно-решающего устройства. В упомянутых работах используются уравнения типа уравнений простой теории Б. П. Никольского для двух ионов уравнение ( 9) ( стр. [14]
Из материала, изложенного в этом разделе, следует, что поведение стеклянного электрода как в кислой, так и в щелочной областях подобны и объясняются ионным обменом. Отклонения от водородной функции в щелочной области объясняются адсорбцией поверхностью стекла катионов, соответственно отклонения в кислой области объясняются адсорбцией поверхностью стекла анионов. Адсорбция катионов и анионов происходит по ионно-обменному механизму. [15]
Страницы: 1 2 3