Объемное поведение
Cтраница 2
В сообщении [46] приводятся данные об объемном поведении чистого этана в гомогенной области и на кривой фазового равновесия вблизи критической точки. Исследованный этан предварительно очищали сорбционным методом на искусственных цеолитах. [16]
Почти ничего не сделано в области изучения объемного поведения расслаивающихся газовых смесей. Между тем данные об объемном поведении представляют большой интерес для теории растворов и критических явлений. Обладая такими данными, можно решить, какие методы предвычисления условий расслоения пригодны для практического применения, какие модели межмолекулярного взаимодействия ( положенные в основу рассуждений) ближе всего отвечают физической реальности. [17]
Кричевского в основном посвящены фазовым равновесиям и объемному поведению растворов при высоких и сверхвысоких давлениях. [18]
Настоящая работа является продолжением исследования [1 - 3] об объемном поведении чистых газов при давлениях до 10000 ат и высоких температурах. [19]
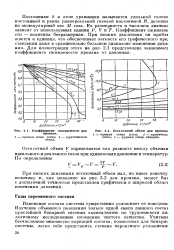 |
Коэффициент сжимаемости для пропана.| Остаточный объем для пропана. [20] |
Изменение состава системы существенно усложняет ее поведена Изучение объемного поведения только одной смеси данного состав простейшей бинарной системы эквивалентно по трудоемкости ан; логичному исследованию поведения чистого вещества. [21]
Мы уже знаем, тем не менее, что объемное поведение систем вблизи критической точки азеотропа очень сильно отличается от поведения вблизи критических точек других смесей. Поэтому представляет интерес проанализировать вопрос о том, почему эти особенности не проявляются в форме критической кривой. [22]
Члены уравнения (11.23) могут быть определены на основании данных объемного поведения и составов равновесных фаз. Тем самым устанавливается согласованность этих данных. Для оценки согласованности данных по фазовым равновесиям требуется интегрирование характеристик объемного поведения. Интегрирование, как указано выше, выполняется при соответствующих составах в точках росы и кипения. Непосредственно из ограничения, накладываемого на парциальные величины, следует, что если уравнение (11.23) справедливо для одного компонента бинарной смеси, то оно справедливо и для другого. Члены в скобках уравнения (11.23) трудно оценить, если состав в точке росы или в точке кипения приближается к чистому компоненту. Определение входящих в это уравнение величин предполагает достаточную точность исходных данных. Кроме того, для оценки интеграла при составе, соответствующем составу в точке кипения, необходимо располагать этими данными как в однофазной, так и в двухфазной области. [23]
Работы школы И. Р. Кричевского в основном посвящены фазовым равновесиям и объемному поведению растворов при высоких и сверхвысоких давлениях. [24]
Поэтому аппараты переменного объема могут быть использованы одновременно для определения объемного поведения смеси и растворимости газа в жидкости. [25]
Для определения химического потенциала с помощью общего предельного метода, необходимо знать объемное поведение системы. [26]
Нужно отметить, что вообще до сравнительно недавнего времени исследованию и обсуждению объемного поведения систем с езеотропами при высоких давлениях в критической области внимания почни не уделялось. Поведение же это весьма своеобразно. Как показали позднейшие работы, это своеобразие очень существенно сказывается на термодинамике систем с азеотропами также и в закритичеокой области. [27]
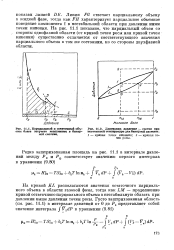 |
Парциальный и остаточный объемы более летучего компонента в бинарной системе.| Диаграмма давление - состав при постоянной температуре для бинарной системы. [28] |
Линия FG отвечает парциальному объему в жидкой фазе, тогда как FH характеризует парциальное объемное поведение компонента 1 в нестабильной области при давлении ниже точки кипения. На рис. 11.1 показано, что парциальный объем со стороны однофазной области ( от кривой точек росы или кривой точек кипения) существенно отличается от соответствующего значения парциального объема в том же состоянии, но со стороны двухфазной области. [29]
Автоклав Боль-сий необходимо, кроме данных о растворимости, иметь еще данные по объемному поведению растворов под давлением. [30]
Страницы: 1 2 3 4