Объемное поведение
Cтраница 3
Для расчета парциального мольного объема компонента раствора и коэффициента а необходимы сведения об объемном поведении системы в гомогенной области существования. [31]
Возможность его использования зависит от точности, с которой уравнение состояния идеального газа описывает объемное поведение вещества. [32]
Часто для этой цели используют обобщенное уравнение состояния, которое позволяет получить количественные характеристики объемного поведения газа с помощью достаточного числа переменных, необходимых для установления состояния системы. [33]
Полученные данные показывают, что уравнение Тэта может быть применено не только для описания объемного поведения сжатой двуокиси углерода, но и для вычисления ее термодинамических свойств. [34]
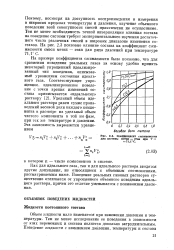 |
Коэффициент сжимаемости. [35] |
Поэтому, несмотря на доступность воспроизведения и измерения в широких пределах температуры и давления, изучение объемного поведения всей совокупности смесей практически не осуществимо. Тем не менее необходимость точной интерполяции влияния состава на поведение системы требует экспериментального изучения достаточного числа различных смесей в широком диапазоне изменения составов. На рис. 2.3 показано влияние состава на коэффициент сжимаемости смеси метан - этан для ряда давлений при температуре 71 1 С. [36]
Тогда механическая модель, состоящая из соединенных параллельно упругой пружины и вязкого амортизатора с присоединенным к ним последовательно другим амортизатором, дает наиболее удобное представление объемного поведения любого материала. [37]
Для того чтобы поставить па твердую термодинамическую основу обобщения по равновесию жидкость - пар многокомпонентных углеводородных систем, представляется желательным изучать фазовые равновесия совместно с объемным поведением систем. [38]
Для того чтобы поставить на твердую термодинамическую основу обобщения по равновесию жидкость - пар многокомпонентных угле-зюдородных систем, представляется желательным изучать фазовые равновесия совместно с объемным поведением систем. [39]
Геологические и промысловые материалы свидетельствуют о том, что залежь имеет волюметрический режим; приток воды в ней ничтожен, потому все расчеты основаны на объемном поведении пласта. [40]
Показано, что в интервале температур 100 - 200 С и np i давлениях до 100 атм объемы жидкой фазы на линии насыщения можно рассчитывать по данным об объемном поведении двойных систем адиподинитрпл - - аммиак и аммиак - вода по уравнению Крпчевского. [41]
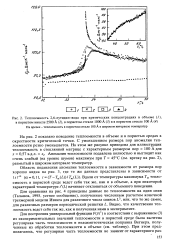 |
Теплоемкость 2 6-лутидин-вода при критических концентрациях в объеме ( 1. [42] |
Вдали от температуры максимума Тт теплоемкость в пористой среде ведет себя так же, как и в объеме, а при некоторой характерной температуре f ( L) начинает отклоняться от объемного поведения. [43]
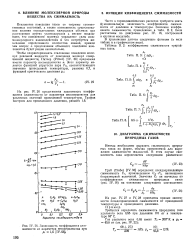 |
Зависимость коэффициента сжимаемости от параметра несовершенства при Рг 1 6 [ IV. 68 ]. [44] |
Отклонение поведения газов от теоремы соответственных состояний, а также возможность существования явления отрицательных кажущихся объемов при растворении других углеводородов в метане показывают, что поведением молекул управляют силы межмолекулярного взаимодействия и что потребуется накопление определенного количества знаний, прежде чем вопрос о предсказании объемного поведения компонентов будет решен окончательно. [45]
Страницы: 1 2 3 4