Коррозионное поведение
Cтраница 1
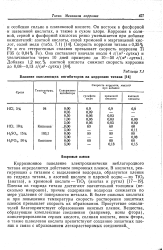 |
Влияние окисляющих ингибиторов на коррозию титана. [1] |
Коррозионное поведение электрохимически неблагородного титана определяется действием покровных пленок. Пленки из гидрида титана достигают значительной толщины ( несколько микронов), причем содержание водорода снижается по мере удаления от поверхности металла. В более сильных кислотах и при повышении температуры скорость растворения защитных пленок превышает скорость их образования. Присутствие окислителей благоприятствует образованию окисных пленок. Вещества, образующие комплексные соединения ( например, ионы фтора), концентрированная серная кислота, соляная кислота, ионы фтора, а также щавелевая кислота препятствуют созданию защитных пленок в связи с образованием легкорастворимых соединений. [2]
Коррозионное поведение в этой среде иллюстрируется рис. 1.18 и 1.19. Пассивное состояние в соляной кислоте возможно ( с теми же оговорками, что и для серной), но анодная защита как током от внешнего источника, так и добав - ками окислителей не дает положительного эффекта и, даже более того, может приводить к отрицательным последствиям. [4]
Коррозионное поведение в промышленных атмосферах различается не так сильно, а кроме того, практическая ценность более высокой коррозионной стойкости материала значительно снижается в условиях, когда изделия находятся в электрическом контакте с другими, более катодными металлами. Например, стальные болты, даже оцинкованные или кадмированные, оказывают значительно более сильное влияние на коррозию магния в местах соединений, чем повышенное содержание локальных катодов в менее чистых сплавах. [5]
Коррозионное поведение всех перечисленных материалов можно считать примерно одинаковым, за исключением припоев и подшипниковых сплавов. Широкий диапазон изменения состава и особые условия эксплуатации этих сплавов требуют дополнительных замечаний. Свойства покрытий основываются на поведении компактного олова. [6]
Коррозионное поведение бериллия в среде СО2 под облучением зависит главным образом от размерных изменений материала в результате распухания. [7]
Коррозионное поведение покрытий сходно с поведением металлического цинка, но при этом наблюдается влияние толщины и строения отдельных слоев покрытия. [8]
Коррозионное поведение магния определяется, с одной стороны, его большой термодинамической активностью, а с другой, - высокой склонностью к пассивации, но недостаточной стойкостью пассивной оксидной пленки к ионам хлора. [9]
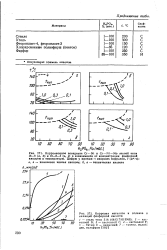
Коррозионное поведение Cr - N1 и Сг - N1 - Mo эмлей липа 18 - 8 ( а, б) и 18 - 8 - 3 ( в, е) в завиоимоети он концентрации фовфорной киолотш и температуры. [11]
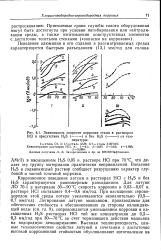 |
Зависимость скорости коррозии стали в растворах НС1 в присутствии H2S ( - - - - - - - - и без H2S ( - - - - - - - - от температуры. [12] |
Коррозионное поведение латуни в растворах НС1 с H2S и без H2S характеризуется равномерным разъеданием. Легирование латуни мышьяком, производимое для обеспечения стойкости к обесцинкованию со стороны охлаждающей воды ( см. гл. [13]
Коррозионное поведение покрытия в общем соответствует поведению компактного металла, но на него оказывают влияние толщина и строение слоев, В случае существования фаз пленки образуются легче, чем на компактном металле. Коррозия при этом замедляется. [14]
Коррозионное поведение покрытий сходно с поведением металлического цинка, но при этом наблюдается влияние толщины и строения отдельных слоев покрытия. [15]
Страницы: 1 2 3 4