Анодное поведение
Cтраница 3
В стационарных условиях растворения анодное поведение латуней определяется поверхностным слоем, обогащенным медью. [31]
Исследовано влияние напряжении на анодное поведение сварных образцов сталей в различных характерных зонах сварных соединений: шва, термического влияния и металла, не подверженного термическом; влиянию. Показано, что наибольшее влияние напряжений на анодное поведение сталей проявляется в зоне термического влияния. Проведены сравнительные испытания сталей ОХ18НЮТ, ЭП-53, ЭП-54 на восприимчивость к коррозионном; растрескиванию при анодной потенциостатической поляризации в растворе щелочи с хлоридом. [32]
На основании результатов исследования анодного поведения алюминия в кислых электролитах ниже предлагается метод контроля и подбора оптимального режима электрополирования. [33]
В связи с изучением анодного поведения кислот представляет интерес ацетилирование, которое, как установлено, происходит при электролизе моно -, ди - или трифенилуксусных кислот в среде уксуснонатриевой соли и уксусной кислоты. [34]
Ранее [1,2] при исследовании коррозионного и анодного поведения титана в растворах хлорной кислоты, содержащих фтористоводородную кислоту, была показана возможность использования титана как анодного материала гальванических элементов. [35]
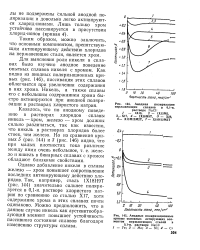 |
Анодные поляризационные кривые основных легирующих элементов нержавеющих сталей в. [36] |
Казалось, что по анодному поведению в растворах хлоридов сплавы никель - хром, железо - хром должны сильно различаться, так как известно, что никель в растворах хлоридов более стоек, чем железо. [37]
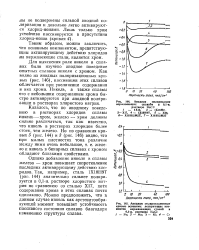 |
Анодные поляризационные кривые основных легирующих элементов нержавеющих сталей в 0 1 - н. растворе NaCI. [38] |
Казалось, что по анодному поведению в растворах хлоридов сплавы никель - хром, железо - хром должны сильно различаться, так как известно, что никель в растворах хлоридов более стоек, чем железо. [39]
Изучено влияние ряда факторов на анодное поведение в условиях выделения С12 модельной системы состоящей из ниролитичес-кой пленки Со о. Температурный интервал 250 - 350 С является оптимальным для получения fi / co o, - анодов обладающих максимальной активностью. Кинетика накопления тю практически подчиняется такому же параболическому закону, как и кинетика роста окисной пленки на чистом Ti. Вследствие этого переходной слой в любом случае должен иметь ограниченную ширину. Отклонения стационарных поляризационных кривых от тафелевской зависимости ( наклон 40 - 2 мВ) при сравнительно высоких плотностях тока не связаны с кинетическими или [ иффуяипннмпг затруднениями, а полностью контролируются омическими погрешностями локализованными не только в объеме активного слоя и в растворе электролита, но в значительной степени и в переходном слое. Температура прогрева пленок и предварительная подготовка поверхности титановой пластинки ( химическое травление в кислотах, пескоструйная обработка) оказывают влияние на фактор шероховатости покрытия, что следует учитывать при сопоставлении скорости анодной реакции на различных образцах. [40]
Два фактора определяют в основном анодное поведение - это-потенциал и отношение концентраций анионов молекул и воды в слое, примыкающем к поверхности металла. Это отношение может существенно отличаться от соответствующего отношения в объеме раствора. Влияние [137] этих двух переменных на широкую гамму возможных реакций представлено на фиг. Диаграмма разделена на четыре области, относительные размеры которых, зависят от металла и участвующих анионов. [41]
Влияние состава стали на ее анодное поведение в серной кислоте изучалось многими авторами и разбирается в ряде обзоров [9, 10, 54, 55]; подробное обсуждение этого вопроса не входит в задачи данной статьи и здесь уместно упомянуть лишь основные данные, по которым можно судить о влиянии легирующих компонентов на параметры анодной кривой, а следовательно, и на параметры анодной защиты. [42]
С этой целью было изучено анодное поведение алюминия в этих электролитах в условиях электрополирования. [43]
Якобсен и Савьер [63] исследовали анодное поведение оксалата в диметилсульфоксиде. [44]
Потенциостатический метод используют при изучении анодного поведения и пассивации металлов и определении энергии активации электрохимических реакций. [45]
Страницы: 1 2 3 4