Поверхность - металл
Cтраница 1
Поверхность металлов можно увеличить, приготовляя их в очень тонко измельченном виде. [1]
Поверхность металлов, за редкими исключениями, можно описать достаточно хорошо с учетом структуры двух ближайших к поверхности атомных слоев. [2]
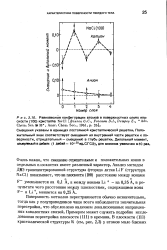 |
Равновесные конфигурации атомов в поверхностных слоях плоскости ( 100 кристалла Nad [ Benson G.C., Freeman D.I., Dempey E., Adv. Chem. Ser. № 33, Amer. Chem. Soc., 1961, p. 26 ].. [3] |
Поверхность металлов перестраивается обычно незначительно, тогда как у полупроводников чаще всего наблюдается значительная перестройка, что обусловлено наличием локализованных направленных ковалентных связей. Примером может служить подробно исследованная перестройка плоскости ( 111) в кремнии. [4]
Поверхность металла представляется как совокупность участков, размеры которых во много раз больше толщины двойного электрического слоя, существующего на границе металла с электролитом. Для таких участков металла остаются правомерными понятия электрод, электродный потенциал. Абсолютные размеры участков достаточно малы и в их пределах физико-химические свойства металла и электролита постоянны. Анодная и катодная реакции идут ро, гомогенному механизму, при однородной поверхнос. [5]
Поверхность металла под гуммирование не должна иметь раковин, трещин, забоин и других подобных дефектов. Дефектные места следует устранять наплавкой металлом с последующей зачисткой. [6]
 |
Ротор центрифуги типа ФМБ.| Корпус центробежного насоса. [7] |
Поверхность металла очищают от смазки, ржавчины, окалины и других загрязнений. [8]
Поверхность металла должна быть обезжирена. [9]
Поверхность металла обладает следующим очевидным свойством: она является эквипотенциальной поверхностью. Действительно, в обратном случае электрические заряды перемещались бы по поверхности проводника. Отсюда следует, что линии силового потока, выходящего с поверхности металла во внешнее пространство, должны образовывать в точках поверхности прямой угол с ней. Так как весь поток выходит из поверхности в одну сторону, то от единицы площади поверхности, согласно закону Гаусса, должно выходить фа линий. [10]
Поверхности металлов и ионных твердых тел по своей природе обладают высокой химической реакционной способностью. Причина этого явления понятна. Структура кристалла в объеме такова, что каждый атом внутри него имеет наилучшие условия для связывания с окружающими его соседними атомами в любом из трех измерений. Но на поверхности способность атомов к связыванию не исчерпывается полностью, поскольку по крайней мере с одной стороны у них нет соседей. Таким образом, поверхность представляет собой область особых химических свойств, которые очень интересны для химиков. Важность таких особых свойств переоценить трудно. Например, коррозия, конечно, протекает на поверхности железа, оказывая одинаково плохое воздействие и на огромную Эйфелеву башню и на маленькую иголку. Оценки показывают, что коррозия ежегодно обходится США в миллиарды долларов. На поверхности алюминия протекает очень быстрая реакция с кислородом воздуха. В результате образуется защитная пленка из весьма инертного оксида. Поэтому мы спокойно пользуемся на кухне алюминиевой фольгой, хотя известно, что при достаточно высокой температуре сам алюминий воспламеняется. Но самое большое внимание химия поверхности привлекает в связи с тем, что именно поверхности могут обладать чрезвычайно высокой каталитической активностью. Способность поверхности твердого тела на несколько порядков увеличивать скорость химических реакций, оставаясь при этом неизменной, называется гетерогенным катализом. III-B мы уже отмечали очень большое значение гетерогенного катализа, на котором основаны промышленные процессы, имеющие чрезвычайно важное экономическое значение. Это одна из самых важных и быстро развивающихся передовых областей химии. [11]
 |
Взаимодействие натрия и калия с водой ( или концентрированной соляной кислотой. [12] |
Поверхность металла сохраняет металлический блеск в течение нескольких дней. Если же концы трубки оттянуть и наглухо заплавить, то получится постоянный образец натрия или калия, который может быть использован в течение многих лет. [13]
Поверхность металла до блеска очищают напильником или наждачной бумагой. [14]
Поверхность металла в реальных условиях применения инструмента в буровой технологии всегда покрыта пленкой окислов. Это значительно осложняет электронную структуру поверхностей и может существенно видоизменить взаимодействие их с ПАВ. Например, по оценкам некоторых авторов коэффициент диффузии водорода в окислы металла на семь порядков ниже, чем непосредственно в металл. [15]
Страницы: 1 2 3 4 5