Поверхность - платина
Cтраница 4
Так, на поверхности платины в некоторых анодных реакциях может образоваться слой смолообразных продуктов, который изолирует электрод от раствора. [46]
 |
Схематическое представление каталитического действия поверхности платины на процесс гидрирования олефинов путем связывания и соединения реагентов. [47] |
Пустым прямоугольником обозначена поверхность платины. [48]
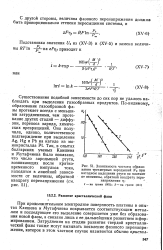 |
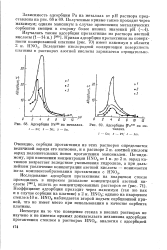
Зависимость частоты образования трехмерных зародышей N при катодном выделении ртути на платине от величины, обратной квадрату перенапряжения ц. [49] |
При продолжительном электролизе поверхность платины в опытах Каишева и Мутафчиева покрывается соответствующим металлом и последующее его выделение совершается уже без образования новой фазы, а связано лишь с ее дальнейшими развитием и формированием. [50]
 |
Адсорбция [ Ра233 на металлах. [51] |
Вследствие кислородной поляризации поверхность платины в растворах азотной кислоты заряжается отрицательно. [52]
Кислород садится на поверхность платины в виде ионов О а водород не удерживается прочно этой поверхностью ( Лэнг - м ю р) и проникает внутрь решетки платины, где под влиянием ударов электронов ( электронного газа) платины он расщеплятся на электроны и протоны. Такое расщепление подтверждается тем, что при пропускании тока через палладий, насыщенный водородом, последний движется к катоду. Протоны выходят на поверхность и там соединяются с ионами О, сначала в ОН -, оставаясь на поверхности платины, а затем в Н2О, которая отрывается от поверхности катализатора. [53]
Предположим, что поверхность платины состоит из N участков, которые отличаются друг от друга величиной энергии активации адсорбции; при этом энергия активации Ел имеет для всех участков одинаковое значение. [54]
Водород адсорбируется на поверхности платины и в таком состоянии легко распадается на атомы, которые могут переходить в раствор в виде ионов Н, оставляя в платине электроны. [55]
Ввиду наличия на поверхности платины атомов со свободными валентностями, в первую очередь происходит активированная адсорбция кислорода, определяемая электронной связью. [56]
 |
Влияние потенциала на скорость. [57] |
Структура оксидных слоев на поверхности платины и ее коррозионная стойкость зависят от соотношения концентраций НС1О4 и НС1 в электролите. [58]
Вследствие того что на поверхности платины находятся атомы со свободными валентностями, в первую очередь происходит активированная адсорбция кислорода, обусловленная возникновением электронной связи. В результате химического взаимодействия кислорода с поверхностью платины ослабляются связи между атомами в молекулах О2 и образуется перекисный комплекс катализатор - кислород. [59]
То, что на поверхности платины, соприкасающейся с газообразным кислородом, имеется слой кислорода, давно известно; поэтому и присутствие одноатомного слоя на электроде можно считать почти достоверным. Указания на существование слоя водорода на поверхностях, выделяющих этот газ, менее убедительны, но все же можно предполагать, что и этот слой существует. [60]
Страницы: 1 2 3 4 5