Поверхность - родий
Cтраница 1
Поверхность родия обладает очень высокой отражательной способ постью, превышающей 80 % для видимой части спектра. Это несколько ниже, чем у только что отполированного серебра, отражательная способность которого составляет при этих условиях в среднем около 90 V Однако, поскольку серебро в нормальной атмосфере тускнеет, его отражательная способность быстро уменьшается и становится меньше, чем у родия. По этой причине родий широко применяют в качестве прочного материала с высокой отражательной способностью. [1]
Поверхность родия обладает высокой отражательной способностью ( 80 %) для видимой части спектра. [2]
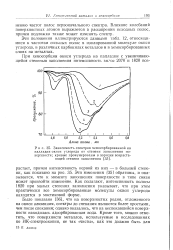 |
Зависимость спектров хемосорбированной на палладии окиси углерода от степени заполнения поверхности. кривые пронумерованы в порядке возрастающей степени заполнения. [3] |
Было показано [36], что на поверхностях родия, отложенного на окиси алюминия, спектры до спекания являются более простыми, чем после спекания; однако оказалось, что на неспекавшейся поверхности находилась адсорбированная вода. [4]
Используя метод, при котором в отличие от метода Эйшенса инфракрасные лучи не проходили через прозрачный образец катализатора, а многократно отражались от каталитической поверхности, Пикеринг и Экстром [ 108а ] обнаружили заметное уменьшение отражаемости от поверхности родия при впуске водорода, а также появление ряда адсорбционных полос, которые они приписали хемосорбированному водороду. [5]
Этилен сильно адсорбируется на всех переходных металлах с большими теплотами адсорбции. С поверхности родия водород вытесняет этилен легче. [6]
Легкость удаления моноксида углерода с поверхности металлического родия и колебательные частоты СО на поверхности, которые близки к его частотам в газовой фазе, показывают, что моноксид связан с поверхностью силами физической адсорбции. Однако если покрыть поверхность родия на 50 % калием в результате его совместной адсорбции с СО, то моноксид углерода становится хемосорбированным. Спектр EELS показывает, что колебательные частоты СО характерны для мостиковой структуры, а связь углерод-кислород становится двойной. Это способствует гидрированию СО, и в этих условиях происходит образование нужных алканов и алкенов ( углеводородов, со -, держащих одну или несколько двойных связей) с большей молекулярной массой ( см. разд. [7]
Как показали проведенные нами ориентировочные опыты, хемосорб-ция этилена при 100 С на поверхности воздушноокисленного порошка родия в присутствии 1 N раствора H2S04 приводит к образованию только этана и углекислого газа. Но этана на поверхности родия образуется значительно меньше, чем на платине, что, как было показано в работе [17], связано с меньшим количеством хемосорбированного на родии водорода. [8]
Легкость удаления моноксида углерода с поверхности металлического родия и колебательные частоты СО на поверхности, которые близки к его частотам в газовой фазе, показывают, что моноксид связан с поверхностью силами физической адсорбции. Однако если покрыть поверхность родия на 50 % калием в результате его совместной адсорбции с СО, то моноксид углерода становится хемосорбированным. Спектр EELS показывает, что колебательные частоты СО характерны для мостиковой структуры, а связь углерод-кислород становится двойной. Это способствует гидрированию СО, и в этих условиях происходит образование нужных алканов и алкенов ( углеводородов, содержащих одну или несколько двойных связей) с большей молекулярной массой ( см. разд. [9]
Считают [6], что депассивирующее действие переменного тока определяется тем, что водород, выделяющийся во время катодного периода, связывается с адсорбированным кислородом. Это приводит к полной или частичной депассива-ции поверхности родия. Во время анодного периода родий 4астично переходит в раствор, успевая вновь запассивиро-ваться. Депассивация наступает при следующем катодном периоде. [10]
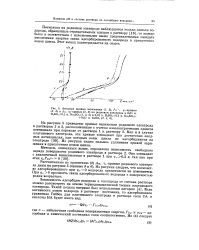
Из рисунка следует, что количество адсорбированного при рг 0 водорода практически не изменяется. При ф г 0 прочность связи адсорбированного водорода с поверхностью родия возрастает. [12]
 |
Зависимость адсорбции метанола от потенциала родиевого электрода в растворе 0 5 М CHgOH 1 N H2S04 при 40 С. [13] |
Для выяснения механизма процесса окисления существенное значение имеет определение природы частицы, адсорбирующейся на поверхности родия из растворов метанола. [14]
Подтверждено, что растворение металлического родия происходит в положительные полупериоды переменного тока. Это позволяет предположить, что депассивирующее действие переменного тока связано с взаимодействием водорода, выделяющегося электролитически, с кислородом, адсорбированным на поверхности родия. [15]
Страницы: 1 2