Заряженная поверхность - металл
Cтраница 1
Заряженная поверхность металла и слой удержанных около нее в растворе ионов противоположного знака образуют две обкладки двойного электрического слоя ( фиг. [1]
 |
Движущаяся капля ртути. [2] |
Заряженная поверхность металла уменьшает свое поверхностное натяжение в зависимости от величины заряда единицы поверхности р и разницы потенциала & на границе между металлом и слоем ионов. [3]
Между положительно заряженной поверхностью металла и электронным облаком возникает электрическое поле. Электрон, покидающий металл, должен преодолеть задерживающее поле этого двойного слоя зарядов. [4]
В этих условиях положительно заряженная поверхность металла, полученная в условиях анодного растворения, способствует увеличению миграции С1 -, которые притягиваются металлом для поддержания электронейтральности ( для компенсации образующегося заряда), что приводит к более высокой концентрации ионов хлора ( С1 -) на поверхности раздела металл / раствор с соответствующим увеличением скорости образования питтингов и их роста на поверхности изучаемого металла. [6]
Полислои ПАВ адсорбируются на положительно заряженной поверхности металла за счет электростатического притяже-жения органических анионов. Углеводородные хвосты ПАВ надстроены солюбилизированными молекулами углеводорода. На границе этой пленки с кислотой сосредоточен монослой молекул ПАВ, ориентированный своими гидрофильными группами SOi в кислую фазу эмульсии. [7]
В результате электростатического взаимодействия между заряженной поверхностью металла и ионами противоположного знака, находящимися в растворе, образуется двойной электрический слой. [8]
Перешедшие в электролит ионы притягиваются электростатическими силами к заряженной поверхности металла и, благодаря этому, не удаляются от нее, а скапливаются у поверхности. Поэтому в слое электролита, непосредственно прилегающем к поверхности металла, из-за наличия излишних ( перешедших) ионов металла появляется избыточный положительный заряд. На границе металл - электролит возникает ионный двойной электрический слой. [9]
В отсутствие специфической адсорбции двойной слой можно уподобить плоскому конденсатору, одной обкладкой которого служит заряженная поверхность металла М, а другой - эффективная граничная поверхность при К. Между металлом и раствором создается скачок потенциала. Электрод обменивается катионами с раствором при любом установившемся скачке потенциала. Ток ионов из металла в раствор равен их току из раствора в металл и равнозначен токам электронов из раствора в металл и из металла в раствор. Силу этого тока, отнесенную к единица поверхности электрода, называют током обмена. Ток обмена считают стандартным / о при средней ионной активности раствора, равной единице ( стр. [10]
В случае, если энергия кристаллической решетки больше энергии гидратации, поверхность металла приобретает положительный заряд вследствие выделения на ней катионов из раствора. Положительно заряженная поверхность металла отталкивает в растворе катионы и притягивает анионы. В результате возникает двойной электрический слой, препятствующий дальнейшему осаждению катионов на поверхности металла, и возникшая разность потенциалов между металлом и раствором уравновешивает разницу между энергией кристаллической решетки и энергией гидратации. [11]
Согласно этому представлению, в случае границы металл - раствор заряженная поверхность металла притягивает из раствора эквивалентное по числу зарядов количество ионов противоположного знака, и все эти ионы вплотную приближаются к поверхности. [12]
 |
Распределение потей - Инала в плотной и диффузной. [13] |
Согласно этому представлению, в случае границы металл - раствор заряженная поверхность металла притягивает из раствора эквивалентное по числу зарядов количество ионов противоположного знака, и все эти ноны вплотную приближаются к поверхности. [14]
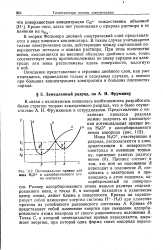 |
Потенциальные кривые для иона Н3О и адсорбированного атома водорода. [15] |
Страницы: 1 2
