Повышение - порядок - реакция
Cтраница 1
Повышение порядка реакции по концентрации комплексного иона, по-видимому, вызвано вступлением оксред-процесса. [1]
Тогда лимитирующим этапом становится диффузия серы и это приводит к замедлению процесса в целом, что выражается повышением порядка реакции. [2]
Для реакции нулевого порядка ( линия 0) скорость не изменяется со временем. При повышении порядка реакции увеличивается влияние концентрации реагента на скорость процесса. [3]
При переходе во внутренне-диффузионную область наблюдаемая скорость процесса снижается вследствие участия в катализе лишь небольшой доли внутренней поверхности и подстраивания скорости реакции к скорости переноса в порах. Как указывает Ройтер [652], с повышением порядка реакции влияние внутренне-диффузионных факторов возрастает. Однако чем больше порядок реакции, тем резче снижается ее скорость в ходе процесса [385], поэтому становится более вероятным выход из диффузионной области при больших степенях превращения, как и при торможении продуктом реакции. [4]
 |
Отношение FCM / FB / ( U. n. [5] |
Числовой анализ этих выражений показывает, что за исключением реакций нулевого порядка ( п 0) при данной интенсивности питания для реактора с идеальным продольным смешением ( мешалка или очень сильная осевая диффузия) всегда требуется больший объем FCM, чем для реактора с поршневым режимом питания. Влияние продольного смешения становится особенно заметным при повышении порядка реакции п и желательной степени превращения V. Изложенное иллюстрируется следующим примером. [6]
Поскольку время пребывания прямо пропорционально объему аппарата, то необходимый объем реактора идеального перемешивания всегда больше объема реактора идеального вытеснения. При равных объемах степень превращения ХА в реакторе идеального вытеснения достигает больших значений, чем в реакторе идеального перемешивания. Следует отметить, что отношение объемов реакторов увеличивается с повышением порядка реакции. [7]
Установлено, что кинетические характеристики реакции германия с хлором зависят от чистоты металла и наличия каталитических добавок. Чем чище металл, тем выше температура начала хлорирования. Наличие примесей ( например, меди) способствует повышению реакционной способности германия, что проявляется в уменьшении энергии активации и в повышении порядка реакции по хлору. [8]
 |
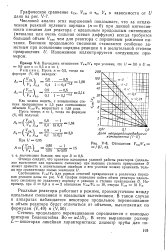
Зависимость коэффициента ускорения массопередачи f от безразмерного времени 6Ь и порядок реакции по хемосорбенту ( 5 при К 2. [9] |
Как видно из рис. 2.1, независимо от величины константы равновесия Л коэффициент ускорения является монотонно возрастающей функцией параметра ( или 6), причем величина - у тем выше, чем больше М и К. Расчеты показывают, что при - оо значение у приближается к асимптотическому значению коэффициента ускорения, соответствующему протеканию мгновенной обратимой реакции. Качественно характер кривых y ( R) не зависит от порядка реакции по хемосорбенту. Влияние р ( при R const) проявляется через различную структуру множителей d, С2 и z и сохраняется при протекании мгновенной реакции. Чем выше р, тем меньше коэффициент ускорения, что связано с большим исчерпыванием хемосорбента вблизи границы раздела фаз при повышении порядка реакции по хемосорбенту. Сравнение проводится при R const. Поэтому увеличение р означает уменьшение рж ( если Вж1), что также сказывается на уменьшении коэффициента ускорения. [10]
Дальнейшая судьба окклюдированных радикалов зависит от физич. В среде осадителя растущие радикалы сворачиваются в достаточно плотные клубки, и активный конец радикала оказывается спрятанным внутри клубка. Кроме того, клубки коагулируют, образуя осадок полимерной фазы. Это приводит к увеличению как средней концентрации радикалов в системе, так и в особенности их концентрации в частицах полимера. Обрыв цепи происходит либо в результате взаимодействия застрявших радикалов с более подвижными радикалами, приходящими из объема жидкой фазы, либо в результате полного захоронения застрявших радикалов в массе полимора. Наблюдаемое часто повышение порядка реакции инициирования по сравнению с гомогенной полимеризацией в жидкой фазе указывает на преобладание второго механизма. Скорость роста цепи с участием окклюдированных радикалов также несколько замедляется вследствие замедленной диффузии мономера внутрь полимерных клубков. Но этот эффект, как правило, перекрывается значительно большим снижением скорости обрыва цепей. Поэтому общая скорость реакции при переходе от гомофазной к гетерофазной полимеризации обычно возрастает. При очень малых скоростях диффузии мо-номера реакция может остановиться полностью. [11]
Дальнейшая судьба окклюдированных радикалов зависит от физич. В среде осадителя растущие радикалы сворачиваются в достаточно плотные клубки, и активный конец радикала оказывается спрятанным внутри клубка. Кроме того, клубки коагулируют, образуя осадок полимерной фазы. Это приводит к увеличению как средней концентрации радикалов в системе, так и в особенности их концентрации в частицах полимера. Обрыв цепи происходит либо в результате взаимодействия застрявших радикалов с более подвижными радикалами, приходящими из объема жидкой фазы, либо в результате полного захоронения застрявших радикалов в массе полимера. Наблюдаемое часто повышение порядка реакции инициирования по сравнению с гомогенной полимеризацией в жидкой фазе указывает на преобладание второго механизма. Скорость роста цепи с участием окклюдированных радикалов также несколько замедляется вследствие замедленной диффузии мономера внутрь полимерных клубков. Но этот эффект, как правило, перекрывается значительно большим снижением скорости обрыва цепей. Поэтому общая скорость реакции при переходе от гомофазной к гетерофазной полимеризации обычно возрастает. При очень малых скоростях диффузии мо-иомера реакция может остановиться полностью. [12]
Страницы: 1