Повышение - предельный ток
Cтраница 1
Повышение предельного тока второй волны на полярограмме щелочного раствора коричного альдегида при добавлении в раствор соли цезия столь значительно, что Барнес и Зуман [208] предложили использовать этот эффект для аналитического определения цезия. [1]
Увеличение суммарной пористости способствует повышению предельного тока заряда, так как соотношение между ними есть величина постоянная. Это создает предпосылки для форсирования процесса заряда до плотности тока. [2]
Общее увеличение равновесной концентрации дырок вызывает повышение предельного тока диффузии дырок. [3]
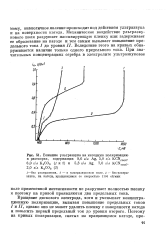 |
Влияние ультразвука на катодную поляризацию в растворах, содержащих 9 6 г. л Ag, 5 0 г / л KCNCBo6, 6 0 г / л К2С03 ( 1 и 2 и 5 3 г / л Ag, 7 0 г / л KCNCBO ( 3, 2 0 г / л К2С03 ( 3. [4] |
Вращение дискового электрода, хотя и уменьшает концентрационную поляризацию, вызывая повышение предельных токов / и II, однако оно не может удалить пленку с поверхности катода и повысить первый предельный ток до уровня второго. [5]
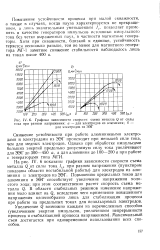 |
Графики зависимости скорости съема металла Q от силы. [6] |
OT силы тока 1ср при разном напряжении ( пунктиром показаны области нестабильной работы) для электродов из алюминия и электродов из ЭЭГ. Повышению предельных токов для алюминия и ЭЭГ способствует увеличение напряжения холостого хода; при этом соответственно растет скорость съема металла Q. В области стабильных режимов изменение напряжения мало влияет на Q, вследствие чего применение повышенного напряжения целесообразно лишь для стабилизации процесса при работе на предельных токах для используемых электродов. [7]
Выявленное влияние борной кислоты на скорость разряда ионов водорода, несомненно, связано с ее буферными свойствами. Некоторое повышение предельного тока палладия ( ветвь / / /) в электролите, содержащем борную кислоту ( см. рис. 90), указывает, что под действием этой добавки увеличивается активная поверхность катода. [8]
Азотнокислый аммоний вводят в электролит с целью повышения предельного тока и увеличения катодного выхода по току. Добавка KN03 способствует улучшению электропроводности и растворению медных анодов. [9]
В настоящее время механизм воздействия ультразвука на химические и электрохимические процессы выяснен недостаточно. Существует лишь ряд предположений. Некоторые авторы отмечают, что ультразвук влияет на энергию дегидратации ионов, способствует преимущественной ориентации ионов и молекул, принимающих участие в электродных реакциях, уменьшению градиента концентрации разряжающихся ионов в прика-тодном слое электролита, повышению предельного тока диффузии и в целом влмя ет на поляризацию электрода. Ультразвук оказывает также диспергирующее и десорбирующее действие при обработке изделий в жидкостях, что может влиять на протекание собственно электрохимической стадии электродного процесса. [10]
Скорость поступления катионов определяется миграцией ( передвижение в результате электростатического взаимодействия), конвекцией и диффузией. Наиболее медленным процессом, определяющим скорость подачи ионов в прикатодное пространство, является диффузия. При повышении плотности тока прикатодный диффузионный слой обедняется ионами осаждаемого металла. Для повышения предельного тока диффузии обычно подогревают электролит и интенсивно его перемешивают, что позволяет увеличить в несколько раз катодную плотность тока и снижает толщину диффузионного слоя з 2 - 3 раза. При наложении ультразвукового поля происходит чрезвычайно интенсивное перемешивание электролита, качественно - отличное от обычного механического или воздушного. Ультразвуковое перемешивание вызывает сильное изменение толщины диффузионного слоя, а после достижения определенной интенсивности - полное его исчезновение. [11]
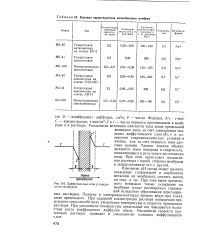 |
Краткая характеристика ионообменных мембран.| Диффузионные слои у поверхности мембраны. [12] |
Изменение рН среды может вызвать осаждение гидроокисей и карбонатов металлов на мембранах, снизить выход по току и пр. При токе выше предельного возможно также осаждение на мембране плохо растворимых соединений вследствие образования пересыщенных растворов. Поэтому в электродиализаторах процесс ведут при токах ниже предельного. При заданной концентрации раствора повышению предельного тока способствует увеличение температуры и скорости протекания раствора. При увеличении температуры предельный ток повышается вследствие роста коэффициента диффузии ионов. Увеличение скорости протекания раствора приводит к уменьшению толщины диффузионного слоя. [13]
В настоящее время механизм воздействия ультразвука на химические и электрохимические процессы выяснен недостаточно. Существует лишь ряд предположений. Очевидно, что влияние ультразвука объясняется кавитационными явлениями, интенсивным перемешиванием при этом жидкости, мгновенно меняющимися перепадами температур и давлений, электрическими явлениями, возникающими при кавитации. Некоторые авторы отмечают, что ультразвук влияет на энергию дегидратации ионов, способствует преимущественной ориентации ионов и молекул, принимающих участие в электродных реакциях, уменьшению градиента концентрации разряжающихся ионов в прика-тодном слое электролита, повышению предельного тока диффузии и в целом влияет на поляризацию электрода. Ультразвук оказывает также диспергирующее и десорбирующее действие при обработке изделий в жидкостях, что может 1влиять на протекание собственно электрохимической стадии электродного процесса. [14]
Следовательно, в течение периода жизни капли изменяется со временем и эффективная величина % - потенциала. Она показала, что предельный ток, ограниченный скоростью рекомбинации анионов фенилглиок-силовой кислоты, резко возрастает при добавлении в раствор небольших количеств поверхностно-активного алкалоида - атропина. При этом начальный участок кривых сила предельного тока - время ( кривых i - t) представляет собой параболу с показателем степени, большим единицы, а в некоторых случаях достигающим даже величины 1 6, тогда как у чисто объемных кинетических токов в отсутствие влияния двойного слоя этот показатель не превышает 2 / а. Повышение предельного тока и быстрый его рост со временем в течение жизни капли при введении в раствор атропина объясняется накоплением на поверхности электрода адсорбированного атропина, приводящим к снижению отрицательного - потенциала со временем и повышению адсорбируемости анионов фенилглиоксиловой кислоты. Наблюдаемый в этом случае очень высокий показатель степени у кривых i - t обусловлен, по-видимому, S-образной формой изотермы адсорбции анионов фенилглиоксиловой кислоты, скоростью рекомбинации которых в адсорбированном состоянии ограничен наблюдаемый кинетический ток, а также S-образной формой изотермы адсорбции атропина. [15]
Страницы: 1 2