Поглощение - анион
Cтраница 1
Поглощение анионов почвой в значительной степени зависит от состава почвенных коллоидов. Опыт показывает, что чем больше в почве содержится глинистых минералов и аморфных полуторных оксидов, тем больше ионов она способна поглотить. [1]
Поглощение анионов почвой в значительной степени зависит от состава почвенных коллоидов. Опыт показывает, что чем больше в почве содержится глинистых минералов и полуторных оксидов, тем больше анионов она способна поглотить. [2]
 |
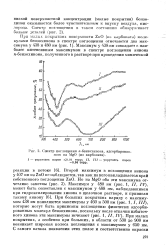
Влияние степени окисления на емкость угля СКТ по натрию ( 7, хлору ( 2, комплексным хлоридным ионам цинка ( 3 и кадмия ( 4. [3] |
Поглощение анионов углями, окисленными в газовой фазе, отмечалось многими авторами [ 13 1в ], которые объясняют этот процесс сорбцией на неокисленных участках угля. [4]
Поглощение анионов протекает медленнее, чем поглощение катионов. [5]
Селективность поглощения разнозарядных анионов зависит как от величины и плотности их заряда, так и от взаимодействия с молекулами воды, определяемого силой соответствующей кислоты. Сравнение селективности поглощения ионов приблизительно одинакового строения и размера показывает ( табл. 25), что с ростом величины заряда селективность поглощения уменьшается, по крайней мере, при обмене больших анионов на сильноосновных анионитах. Следовательно, электростатическое притяжение к фиксированным группам ионита в данном случае не имеет решающего значения. Однако в ряде случаев, например на анионообменном оксиде алюминия, получены ряды селективности с преимущественным поглощением более высокозарядных анионов. [6]
Зависимость селективности поглощения анионов от рассмотренных выше факторов сложнее, чем катионов, так как состав большинства анионов, в том числе комплексных, более сложный, а способность их к гидратации меньшая, чем у катионов. Для простых анионов, например одноатомных, с электронной конфигурацией инертного газа, склонность к гидратации уменьшается с увеличением кристаллографического размера иона; этим обусловлен, например, ряд селективности F - С1 - Вг - 1 - на сильноосновных аниони-тах. Для сложных ионов ( анионов слабых или умеренно сильных кислот) степень их гидратации определяется силой соответствующей кислоты - чем слабее кислота, тем больше склонность аниона к гидратации. [7]
В обоих случаях поглощение анионов происходит в обмен на ионы ОН, которые при кислой реакции отщепляются от молекул, расположенных на поверхности коллоидной частицы. [8]
 |
Спектр поглощения и-бензохинона, адсорбированного на MgO ( из карбоната. [9] |
Второй максимум в поглощении аниона у 407 нм на ZnO не наблюдается, так как на него накладывается край собственного поглощения ZnO. При малых покрытиях, а особенно при больших, в области от 530 до 900 нм возникает широкая полоса поглощения с максимумом у 650 нм. [10]
ИК-спектре не наблюдается полос поглощения анионов, не связанных с катионами. Вследствие этого даже при высокой степени гидратации катионы, по данным ИК-спектров, оказываются связанными преимущественно с окружающими анионами. [11]
Вытесняющее действие гидроксильных ионов затрудняет поглощение анионов. [12]
Слабоосновные аниониты можно использовать для поглощения анионов сильных кислот в присутствии слабых кислот, однако это редко бывает необходимым в химическом анализе. [13]
При обсуждении нричин непостоянства длины волны края поглощения анионов в этих соединениях следует учитывать, конечно, и некоторые специфические особенности последних, проявляющиеся, например, в виде их аномальных электрических и магнитных свойств. [14]
 |
Формы нормальных колебании тетраэдрических частиц. [15] |
Страницы: 1 2 3 4