Поглощение - двуокись - сера
Cтраница 1
 |
Схема извлечения двуокиси серы из газа по цинково-кислотному методу. [1] |
Поглощение двуокиси серы суспензией окиси цинка может быть осуществлено как в барботаж-ных аппаратах, так и в поглотительных башнях с насадкой. При этом окис-ляемость двуокиси серы во втором случае значительно меньше. [2]
Поглощение двуокиси серы из разбавленных сернистых газов производится взвесью измельченного нефелина в воде или в растворе солей натрия и калия. При поглощении часть сернистокислых солей окисляется, как обычно, в сернокислые. [3]
Поглощение двуокиси серы суспензией окиси цинка может быть осуществлено как в барботаж-ных аппаратах, так и в поглотительных башнях с насадкой. При этом окис-ляемость двуокиси серы во втором случае значительно меньше. [4]
Поглощение двуокиси серы из разбавленных сернистых газов производится взвесью измельченного нефелина в воде или1 в растворе солей натрия и калия. При поглощении часть сернистокислых солей окисляется, как обычно, в сернокислые. [5]
Для поглощения двуокиси серы применяют поглотительную склянку емкостью 150 - 200 мл. Входная трубка склянки соединяется со стеклянной пробоотборной трубкой, содержащей гигроскопическую вату в виде плотного тампона для улавливания тумана и брызг кислоты из газа. Второй конец пробоотборной трубки присоединяют к источнику газа. [6]
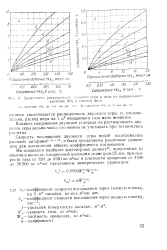 |
Зависимость растворимости ДВУОКИСИ серы в воде от парциального давления SO 2 в газовой фазе. [7] |
Скорость поглощения двуокиси серы водой исследовалась разными авторами2 54 56, и были предложены различные уравнения для вычисления общего коэффициента поглощения. [8]
Спектр поглощения двуокиси серы исследовался начиная с 1914 г. Райтом [1] Гарретом [.], Шефаром [3,4], Ле-Бланом, Кангро и Андрихом [ S ], Дитцелем и Гала-нос [ б ] и Гетманом [ ] в различных условиях. По их данным, интенсивность поглощения водных растворов двуокиси серы не подчиняется закону Бэра; поэтому спектрографическое исследование производилось нами при одинаковых условиях и близких концентрациях, всегда исследовались свежеприготовленные растворы. Были исследованы растворы двуокиси серы в пентане, диэтиловом эфире, этаноле, воде и концентрированной серной кислоте. [9]
Спектр поглощения двуокиси серы в пентане исследован при концентрациях 3 - 10 2 - 3 - 10 - мол. [10]
Спектр поглощения двуокиси серы в диэтиловом эфире исследован при концентрациях 0.5 - 0.5 10 - 3 мол. [11]
Спектр поглощения двуокиси серы в кэнцентрированной серной кислоте исследован при концентрациях 0.67 - 0.67 10 - 3 мол. Вся полоса ( рис. 1, кривая 5) сравнительно с таковой в растворе в пентане, уменьшена в интенсивности максимума в 13 раз. [12]
Спектр поглощения двуокиси серы в пентане с эквимолекулярным количеством этанола исследован при концентрациях 1.1 10 - 1 - 1.1 10 - 2 мол. Максимум полосы ( рис. 2, кривая 3) в 180 раз менее интенсинен по сравнению с таковым в пентане. [13]
Спектр поглощения двуокиси серы в пентане с эквимолекулярным количеством хлористого водорода исследован при концентрациях 10 - 1 - 10 - 2 мол. Максимум полосы ( рис. 2, кривая 4) в 130 раз менее интенсивен, чем таковой в пентане. [14]
Интенсивные полосы поглощения двуокиси серы очень часто появляются в спектрах в качестве загрязнения; они накладываются на спектр испускания большинства пламен, содержащих серу. [15]
Страницы: 1 2 3 4