Поглощение - двуокись - сера
Cтраница 3
Сравнение кривых поглощения диметилсульфита и двуокиси серы в этаноле показывает, что основной характер поглощения двуокиси серы сохраняется в спектре диметилсульфита, но очень ослаблен влиянием третьего атома кислорода, метильных групп и растворителя. Возможно образование продуктов присоединения, чем объясняется и сильное расширение полос в растворах в воде и в пентане. [31]
Предложены также способы получения сернокислого аммония из двуокиси серы путем ее окисления и взаимодействия трехокиси серы с газообразным аммиаком или путем поглощения двуокиси серы водой, взаимодействием сернистой кислоты с аммиаком и последующим окислением сернистокислого аммония кислородом. [32]
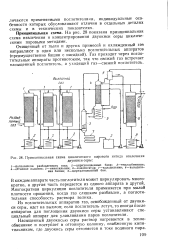 |
Принципиальная схема циклического парового метода извлечения. [33] |
Из поглотительных аппаратов газ, освобожденный от двуокиси серы, идет на выхлоп; если поглотитель летуч, то иногда после аппаратов для поглощения двуокиси серы устанавливают специальный аппарат для улавливания паров поглотителя. [34]
В этих пламенах наблюдаются также не очень интенсивные полосы испускания SO, а в области около 3000 А на спектр испускания обычно накладываются полосы поглощения двуокиси серы. В пламени H2S наблюдаются также полосы ОН при 3064 А, но полоса ( см. стр. А не была обнаружена в этих пламенах. [35]
 |
Способ закрепления капельной воронки в пробке колбы. [36] |
Вульфа, ломещают 50 мл концентрированной серной кислоты для поглощения паров спирта, а в скля нку Вульфа-14 % - ный раствор едкого натра для поглощения двуокиси серы, образующейся в результате побочной реакции. В три следующие склянки, установленные последовательно, наливают по 50 мл хлорсульфоновой кислоты. Выходное отверстие последней склянки защищают от влаги хлоркальциевой трубкой. [37]
Для этого поступают следующим образом: наливают в мерную колбу емкостью 100 мл столько же 3 % - ного раствора перекиси водорода, сколько было взято для поглощения двуокиси серы из газа ( 50 или 60 мл), и разбавляют водой до метки. Из колбы отбирают пипеткой и переносят в пробирку количество раствора, равное количеству исследуемого раствора, взятому для определения, и разбавляют водой до объема 10 мл. [38]
Содержащиеся в грунтовой эмали окислы никеля и кобальта иногда приводят к образованию сульфидов, согласно описанию Штуккерта55, Особенно легко образуется сульфид никеля при восстановлении в атмосфере печи сульфатов щелочей, которые Могут присутствовать в виде загрязнений в шихтных материалах или образоваться в результате поглощения двуокиси серы и кислорода щелочью в расплаве эмали. Сульфиды кобальта образуются значительно труднее, поэтому Штук-керт предпочитает пользоваться для грунтовых эмалей окисью кобальта. [39]
Задняя часть трубки после лодочки с навеской заполняется последовательно: I-слоем крупных частиц окиси меди, предварительно освобожденной от органических примесей прокаливанием в железном тигле ( этот слой закрепляется при помощи дисков медной сетки или рыхлых асбестовых пробок); II - слоем хромата свинца длиной 5 см с размером зерна 2 - 3 мм для поглощения двуокиси серы; III - спиралью из серебряной сетки длиной 8 см для связывания свободных галогенов; IV - блестящей восстановленной медной спиралью для восстановления окислов азота до свободного азота. Медную спираль необходимо вновь восстанавливать перед каждым сожжением. [40]
Что касается загрязнения атмосферы вредными примесями ТЭС и АЭС, то необходимо отметить, что защита окружающей среди от вредных примесей дымовых газов - золы, двуокиси серы, азота и др. - связана со значительным удорожанием 1 кВт установленной мощности, которое составляет 2 - 5 % при затратах на оборудование для улавливания твердых частиц и 25 - 50 % - на установки для поглощения двуокиси серы. Высокая стоимость и пока еще невысокая надежность работы установок по удалению из дымовых газов двуокиси серы обусловливают незначительное применение их на практике и повсеместное использование методов рассеивания примесей в атмосфере. [41]
Кроме того, Зальманг и Беккер изучили вопрос о присутствии в стекле металлов различной степени окисления, которые стремятся к достижению состояния гетерогенного газового равновесия с кислородом атмосферы печи. Поглощение двуокиси серы из атмосферы печи также объясняется абсорбцией тех газов, которые при данных физико-химических условиях вступают в реакцию с расплавом стекла, образуя устойчивые соединения. Так, кислород легко может быть введен в стекло, содержащее закись железа, или Двуокись серы и кислород - в известково-натрие-вые силикатные стекла. [42]
В результате первого этапа сорбции поверхность пятиокиси ванадия покрывается адсорбированными молекулами двуокиси серы, и сорбция приостанавливается. Можно предположить, что поглощение двуокиси серы сможет продолжаться, если образовавшаяся поверхностная пленка разрушится, поверхностные атомы ванадия, связанные с двуокисью серы, отделятся от остальной решетки и образуют кристаллические зародыши новой фазы. Скорость этих процессов определяет величину индукционного периода, предшествующего второму этапу сорбции. В дальнейшем происходит рост кристаллов нового продукта и уменьшение кристаллов пятиокиси ванадия, взаимодействующей с двуокисью серы. Этот процесс и представляет собой второй этап сорбции. [43]
При прокаливании кристаллов во вращающейся печи в токе дымового газа ( температура газа на входе 1000 - 1100, на выходе 400; время пребывания материала в печи 20 мин. Получаемая при прокаливании окись магния способна к поглощению двуокиси серы. [44]
Окисление двуокиси серы вызывается только светом, с длиной волны менее 1860 А. Теллер, Спонер и Франк в 1932 г. р8 ] доказали, что поглощение двуокиси серы в средней ультрафиолетовой области не сопровождается ее диссоциацией. Граница предис-соционной зоны лежит при Х 210 () А. [45]
Страницы: 1 2 3 4