Закись - кобальт
Cтраница 3
При совместном прокаливании закиси кобальта и окиси цинка ( или солей этих металлов и летучих кислот) протекают сложные процессы. Закись кобальта и окись цинка кристаллизуются в различных кристаллических системах: СоО - в кубической, a ZnO - в гексагональной; поэтому они могут образовывать твердые растворы лишь в особых условиях. [31]
При совместном прокаливании закиси кобальта и окиси цинка ( или солей этих металлов и летучих кислот) протекают очень сложные процессы. Закись кобальта и окись цинка кристаллизуются в различных кристаллических системах: СоО - в кубической, a ZnO - в гексагональной, и поэтому они могут образовать твердые растворы лишь в особых условиях. [32]
Окисление окиси углерода на закиси кобальта при низких температурах обнаруживает много общего с реакцией на закиси меди, и механизм с образованием комплекса СО3 здесь также согласуется с экспериментальными данными. [33]
Например, СоО - закись кобальта, Со2О3 - окись кобальта. Однако это правило применяется нестрого. В частности, в тех случаях, когда на один атом элемента в молекуле окисла приходится целое число атомов кислорода, это число может быть указано числительными приставками дву, трех или четырех перед словом окись; например, СО - окись углерода, СО2 - двуокись углерода; WO3 - трехокись вольфрама; RuO4 - четырехокись рутения. [34]
Окисление окиси углерода на закиси кобальта при низких температурах обнаруживает много общего с реакцией на закиси меди, и механизм с образованием комплекса СО3 здесь также согласуется с экспериментальными данными. [35]
Нами разработана методика получения закиси кобальта, основанная на термической диссоциации окиси или закись-окиси кобальта в вакууме и последующем охлаждении закиси в вакууме. [36]
 |
Произведение растворимости Со ( ОН2. [37] |
Она образуется при нагревании закиси кобальта СоО в интервале температур от 400 до 900 С и при сгорании пирофорного кобальта на воздухе. Она получается также при нагревании гидроокиси кобальта. [38]
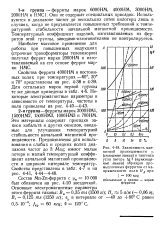 |
Зависимость магнитной проницаемости. А ( сплошные линии и тангенса угла потерь tg 5 ( пунктирные линии образцов промышленных ферритов от напряженности поля Нд при / 100 кгц. [39] |
Эти материалы содержат присадки закиси кобальта и других окислов, вводимые для улучшения температурной стабильности начальной магнитной проницаемости. Предназначены для использования в слабых и средних полях диапазона частот до 3 Мгц; имеют малые потери и малый температурный коэффициент начальной магнитной проницаемости в широком интервале температур. [40]
Кобальт образует следующие окислы: закись кобальта СоО еро-зеленого цвета, окись Со2Оз буро-черного цвета и закись-жись СозО4 черного цвета. ОН) 2 или восстановлением высших окислов в струе водо-ода. [41]
Низшее кислородное соединение кобальта - закись кобальта СоО - представляет собой немагнитный кристаллический порошок кубической структуры, темнозеленого цвета. [42]
Испытать, растворяется ли гидрат закиси кобальта в кислотах и в избытке раствора щелочи. Какими свойствами обладает гидрат закиси кобальта. [43]
Температура к концу осаждения гидрата закиси кобальта должна быть не ниже 70 С. [44]
Испытать, растворяется ли гидрат закиси кобальта в кислотах и в избытке, раствора щелочи. Какими свойствами обладает гидрат закиси кобальта. [45]
Страницы: 1 2 3 4