Закись - титан
Cтраница 1
Закись титана представляет собой не диэлектрик, а полупроводник с высоким углом диэлектрических потерь. Таким образом, наличие восстановительной среды при вжигании серебра может привести к ухудшению электрических характеристик керамического основания. [1]
Закись титана TiO может быть получена нагреванием в вакууме при температуре 1500 - 1600 спрессованной смеси металлического титана и его двуокиси и представляет собой коричневые кристаллы с болотистым оттенком. Это же кислородное соединение титава, но меньшей чистоты, может быть получено нагреванием двуокиси титана TiO2 с магнием, цинком или углеродом. [2]
Соли закиси титана, у которых TI трехвалентен; они непостоянны и окрашены в водном растворе в фиолетовый цвет. [3]
Гидрат закиси титана Ti ( OH) 2 образуется в виде вещества черного цвета при действии щелочей па р-ры солей 2-валентного титана. Соединение неустойчиво и легко окисляется, образуя во влажном воздухе Ti ( OH) 3 фиолетового цвета, переходящий затем в Ti ( OH) 4 белого цвета. [4]
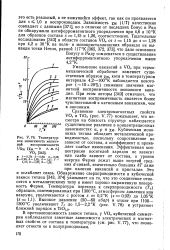 |
Температурная зависимость магнитной восприимчивости. / Хм ( Хм - в м. е. VOS. [5] |
В противоположность закиси титана, у VOS кубической симметрии наблюдаются заметные зависимости электрических и магнитных свойств от состава и температуры ( см. рис. V. [6]
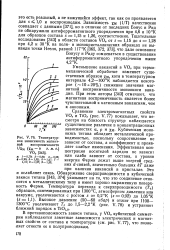 |
Температурная зависимость магнитной восприимчивости. / Хм ( Хм - в м. е. VOS. [7] |
Обнаружение сверхпроводимости в кубической закиси титана [343, 374] указывает на то, что это соединение относится к металлическому типу и имеет хорошо выраженную поверхность Ферми. [8]
Титан образует следующие окислы: ТЮ - закись титана, Ti2O3 - окись титана и ТЮа - двуокись титана. Закись титана - основной окисел; соответствующие ему соли нестойки. [9]
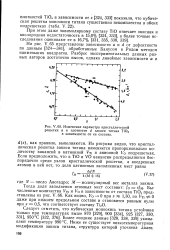 |
Изменение параметра кристаллической. [10] |
Из рисунка видно, что кристаллическая решетка закиси титана изменяется пропорционально количеству вакансий в катионной VTI и анионной VQ подрешетках. [11]
При ответе учтите, что часть титана остается в шлаке в виде закиси титана ТТО и трехокиси титана Ti2O3, которые с окисью алюминия дают соответствующие алюминаты. [12]
Промежуточный окисел Ti3Os и окись Ti2O3 способны растворять закись железа и ильменит, а также образовывать растворы с ТЮ2 и закисью титана ТЮ. Эти реакции приводят к образованию сложных соединений, кристаллизующихся при затвердевании шлаков. [13]
В последних работах для электролитического получения титана рекомендуется электролит из K2TiF6 NaCl, а также электролит на основе расплавленного СаСЬ, в который вводят мелкозернистую закись титана ТЮ. [14]
Закись титана получают нагреванием смеси двуокиси с порошком титана в вакууме при 1550 С, а также восстановлением ТЮ2 магнием, алюминием или углеродом. Закись титана нерастворима в воде. С серной и соляной кислотами она реагирует с выделением водорода и образованием растворов трехвалентного титана. [15]
Страницы: 1 2