Подвижность - молекула - вода
Cтраница 1
 |
Измерение энергии ближайших молекул в окружении некоторых ионов. [1] |
Подвижность молекул воды в окружении этих ионов возрастает, и, таким образом, наблюдается отрицательная гидратация. Знак этой зависимости изменяется между ионом Na с радиусом 0 98 А и ионом К с радиусом 1 33 А. Размеры между этими двумя значениями характерны для ионов, не обнаруживающих ни положительной, ни отрицательной гидратации. Путем измерений магнитной восприимчивости растворов электролитов Ергин и Кострова [96] показали, что переход между положительной и отрицательной гидратацией три комнатной температуре происходит при значении ионного радиуса - 1 1 А. [2]
Подвижность молекул воды увеличивается, но увеличивается и число водородных связей, что приводит к росту энергетического барьера для переориентации и переноса молекул воды. [3]
Оценка подвижности молекул воды вблизи иона производится Самойловым из следующих соображений. Как уже говорилось, молекулы жидкостей, в том числе и молекулы воды, находясь в окружении себе подобных, пребывают в стационарном состоянии в течение среднего времени - с. [4]
Оценка подвижности молекул воды вблизи иона производится Самойловым из следующих соображений. Времени т соответствует энергия активации Е ДЕ. [5]
Уменьшение подвижности молекул воды вблизи неполярной группы, проявляющееся в уменьшении энтропии, часто описывают как образование айсбергов. Этот удобный, но в принципе неверный термин обозначает просто тот факт, что молекулы воды вблизи молекулы растворенного вещества не могут осуществлять либрацию и вращение в такой же степени, как в основной массе растворителя. [6]
Вопрос о подвижности молекул воды на поверхности неорганических окислов был рассмотрен выше. В настоящем разделе обсуждаются проблемы диффузии молекул воды на поверхности разрушения. При этом имеется в виду, что диффузия происходит в узком поверхностном слое: молекулы воды передвигаются от одного центра адсорбции к другому без столкновений с другими молекулами адсорбированной воды. [7]
А поскольку подвижность молекул воды непосредственно отражается в скоростях релаксации ( правда, с некоторыми оговорками [17]), ядерно-релаксационные исследования, видимо, наиболее пригодны именно для подобного подхода к обсуждению результатов. [8]
Адсорбция и подвижность молекул воды в щелевидных микропорах активного угля ( исследование методом Монте-Карло): Препр. [9]
Количественная оценка подвижности молекулы воды проводилась с учетом представлений о том, что молекулы воды совершают в трехмерной смачивающей пленке беспорядочные поступательные и вращательные движения со средним временем корреляции тс. [10]
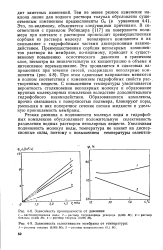 |
Зависимость проницаемости от давления.| Зависимость селективности мембраны от температуры. [11] |
Резкая разница в подвижности молекул воды и гидрофобных комплексов обусловливает положительную селективность разделения водных растворов неполярных веществ. [12]
 |
Схема строения молекулы воды.| Ассоциация полярных молекул. [13] |
В жидком состоянии подвижность молекул воды уменьшается; они образуют группы из 2, 3, 4 молекул и более, состав которых принято обозначать формулой ( H2O) X. Величина х зависит от температуры. В результате меняется плотность воды. [14]
С увеличением расстояния от частицы подвижность молекул воды постепенно возрастает, вследствие чего вокруг частицы образуется пространственная оболочка, называемая гидратной, которая предохраняя частичку от слипания ( коагуляции) с подобными ей, обусловливает устойчивость дисперсной системы - способность сохраняться во взвешенном состоянии. Чем больше гидратирована частичка глины, тем более устойчива суспензия. Степень гидратации частицы возрастает с увеличением электрического заряда, который увеличивается с ростом степени диссоциации. Последняя достигает наибольшей величины в щелочной среде, когда кислотный ион водорода глинистой частицы заменяется более диссоциирующим ионом натрия. [15]
Страницы: 1 2 3 4