Закон - амаг
Cтраница 1
Закон Амага [ равенство (16.12) ] находит практическое применение при объемном анализе смесей идеальных газов. [1]
По закону Амага общий объем V смеси газов, химически не взаимодействующих друг с другом, равен сумме тех индивидуальных объемов Vi, которые занимал бы каждый из этих газов, взятый при той же температуре и под тем же давлением, что и газовая смесь. [2]
Дальтона, закон Амага или правило аддитивности псевдоприве-деппых свойств газовой елеен. [3]
Для идеальных газов закон Амага непосредственно вытекает из их уравнения состояния. [4]
Равенство (2.176) выражает закон Амага. [5]
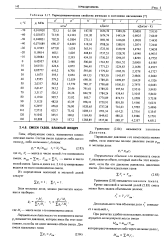 |
Термодинамические свойства аммиака в состоянии насыщения. [6] |
Уравнение (2.85) называется законом Амага. [7]
Такие смеси, подчиняющиеся закону Амага для всех давлений от 0 до р, называются идеальными. Однако закон Дальтона для них в общем случае неприменим. [8]
Это ур-ние выполняется более точн чем закон Амага. [9]
Эти условия сильно ограничивают область применения закона Амага. [10]
Равенство (16.12) служит математическим выражением так называемого закона Амага; он является следствием закона Дальтона. Сравнивая равенства (16.5) и (16.12), легко видеть аналогию между этими законами. [11]
Это ур-ние выполняется более точно, чем закон Амага. [12]
Этот закон аддитивности объемов также известен как закон Амага или закон Ледюка. [13]
Уравнение ( 7 - 10) выражает собой закон Амага. [14]
Уравнение (1.68) выражает закон Дальтона, а уравнение (1.69) - закон Амага. [15]
Страницы: 1 2 3