Закон - дюлонг
Cтраница 1
Закон Дюлонга и Пти, действительно, оказался чрезвычайно важным и весьма своевременным для дальнейшей разработки атомистики, и в особенности для установления правильных атомных весов элементарных атомов. [1]
Закон Дюлонга и Пти имеет приближенный характер. [2]
Закон Дюлонга и Пти является, как мы видели, следствием закона равномерного распределения энергии по степеням свободы. Поэтому тот факт, что твердые тела в действительности не следуют закону Дюлонга и Пти при низких температурах, показывает, что гипотеза о равномерном распределении энергии по степеням свободы является приближением. [3]
Закон Дюлонга и Пти приблизительно верен для ряда веществ. [4]
Закон Дюлонга и Пти сравнительно хорошо подтверждается на опыте при не слишком низких температурах. [5]
Закон Дюлонга и Пти, однако, не выполняется при низких, а для ряда веществ ( бор, алмаз, кремний) и при средних температурах. [6]
Закон Дюлонга и Пти является, как мы видели, следствием закона равномерного распределения энергии по степеням свободы. Поэтому тот факт, что твердые тела в действительности не следуют закону Дюлонга и Пти при низких температурах, показывает, что гипотеза о равномерном распределении энергии по степеням свободы является приближением. [7]
Закон Дюлонга и Пти, как это и следовало ожидать, вскоре после открытия был применен для проверки атомных весов элементов. Это был существен - - ный шаг в развитии атомного учения: исправление атомных весов осуществлялось путем подбора коэффициентов, на которые надо умножить экспериментально найденные данные, чтобы получить правильные величины атомных весов. [8]
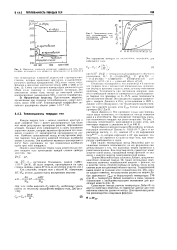 |
Иямомснис плотности различных модификаций SiO. при нагреве, охлаждении и в процессах превращения по данным.| Зависимость атомных тенлоемкостей при постоянном объеме от температуры. [9] |
Закон Дюлонга и Пти применим только при температурах выше комнатных, но оказывается иногда неверным даже и в этой области. При понижении температуры удельная теплоемкость твердых тел резко возрастает. На рис. 1 показаны теплоемкости, приходящиеся на один атом, для некоторых веществ в диапазоне от 0 до 400 К. [10]
Закон Дюлонга и Пти плохо выполняется у кристаллов, составленных из отдельных молекул. Такие кристаллы имеют очень много ветвей колебаний. Одни из них приближенно отвечают колебаниям молекул как целого, другие - внутримолекулярным колебаниям. Для таких ветвей неравенство / icom; 0 не имеет места при комнатной температуре, а при более высоких температурах молекулярные кристаллы обычно уже плавятся или возгоняются. [11]
 |
Молярная теплоемкость некоторых твердых веществ при 25 С. [12] |
Закон Дюлонга и Пти соблюдается для твердых одноатомных тел при достаточно высоких температурах. Для большинства тел такой достаточно высокой температурой является уже комнатная температура. Однако для некоторых тел с малой атомной массой, например для бериллия, бора, углерода ( алмаза), комнатная температура недостаточно высока, и они подчиняются закону Дюлонга и Пти лишь при более высокой температуре. Наоборот, при охлаждении все тела обнаруживают отступления от закона Дюлонга и Пти. При охлаждении теплоемкость всех тел уменьшается. [13]
Вообще закон Дюлонга и Пти для элементов вполне справедлив. Однако существует целая группа элементов, которая одно время наделала много хлопот ученым, так как представляла весьма резкое отступление от этого общего закона. Уголь известен в трех состояниях и эти три его состояния имеют отличную друг от друга теплоемкость. Однако ни одна не подходит для выражения закона Дюлонга и Пти, и все он i представляют весьма резкое отступление. [14]
Однако закон Дюлонга и Пти верен только при достаточно высоких температурах. [15]
Страницы: 1 2 3 4