Закон - кратное отношение
Cтраница 1
Закон кратных отношений состоит в том, что, когда два элемента образуют несколько соединений, массы одного из элементов в разных соединениях относятся, как целые числа. [1]
Закон кратных отношений открыт был в самом начале XIX столетия манчестерским профессором Дальтоном, при исследовании соединений углерода с водородом. Оказалось, что в двух газообразных соединениях этих простых тел, в болотном СН4 и в маслородном С2Н4 газах, на одно и то же количество водорода содержатся количества углерода, кратные между собою; а именно, в болотном газе вдвое меньше углерода, чем в маслородном. Хотя анализ того времени был мало точен, но справедливость закона, узнанного прозорливостью Дальтона, подтвердилась дальнейшими точными исследованиями. Выставив закон кратных отношений, Дальтон дал и гипотетическое или вероятное ему объяснение. Объяснение это основывается на атомической гипотезе строения вещества. В самом деле, закон кратных отношений необыкновенно просто понимается при допущении атомического строения вещества. Формы и свойства веществ определяются расположением атомов в пространстве и их состоянием движения, а явления, совершающиеся с веществами, понимаются как перемещения взаимного положения атомов и как перемены движения, в каком можно предполагать атомы, их группы и совокупности. Родилось атомное представление о веществе еще у метафизиков-идеалистов древности, но до последнего времени оно борется с динамическим представлением, считающим вещество только местом проявления сил или энергий. В новейшее время громадное большинство естествоиспытателей держится атомической гипотезы, но понятия современных атомистов совершенно иные, чем были у философов древности. [2]
Закон кратных отношений, как и закон постоянства состава, неприменим к соединениям переменного состава ( бертоллидам, с. [3]
Закон кратных отношений, как и закон постоянства состава, неприменим к соединениям переменного состава ( бертоллидам, стр. [4]
Закон кратных отношений: если два элемента образуют друг с другом несколько химических соединений, то весовые количества одного из элементов, приходящиеся в этих соединениях на одно и то же количество другого, относятся между собой как простые целые числа. [5]
Закон кратных отношений, к открытию которого был так близок Пруст, был в конечном счете сформулирован Дальтоном, проводившим аналогичные опыты с окислами углерода и азота. [6]
Закон кратных отношений является фактически объединением закона сохранения массы ( см. 2.1) и закона постоянства состава на базе атомной гипотезы строения вещества, а все эти законы послужили основой для формулирования понятия об относительной атомной и молекулярной массе и ознаменовали начало развития химии как количественной науки. [7]
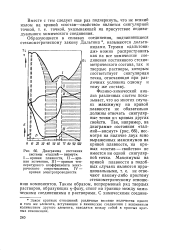 |
Диаграмма состояния. [8] |
Закон кратных отношений: различные весовые количества одного и того же элемента, вступающие в химические соединения с неизменным количеством другого элемента, находятся между собой в простых кратных отношениях. [9]
Закон кратных отношений, который можно формулировать так: если одно тело дает с другим несколько соединений, то эти соединения различаются только количествами второго тела, приходящегося [. . .] на одно и то же количество первого. Эти различные количества второго тела составляют друг с другом весьма простую кратную пропорцию. [10]
Закон кратных отношений был открыт весьма легко при исследовании минеральных тел. За этим законом, который, очевидно, гораздо более сложен, чем все прежде рассмотренные ( так как здесь дело идет о сравнении разнообразных соединений, и должно исследовать, по крайней мере, пары соединений), следует закон паев. [11]
Закон кратных отношений должен получить примерно следующую формулировку. [12]
Закон кратных отношений обычно представляют в учебниках как один из основных законов химии. Однако в действительности неорганических соединений, которые подчиняются этому закону, существует немного. Соединения или, вернее, системы соединений, в которых наблюдаются значительные отклонения от сте-хиометрических соотношений, составляют в неорганической химии скорее правило, чем исключение. Актинидные элементы, подобно другим переходным элементам, обнаруживают такие свойства особенно сильно. Практически все твердые соединения актинидных элементов с полуметаллическими свойствами отклоняются от стехиометрии. Так, большое количество соединений этих элементов характеризуются областью существования стабильных соединений, а не наличием одного единственного соединения с составом, который может быть выражен как отношение малых целых чисел. [13]
Закон кратных отношений, как и закон постоянства состава, не является всеобщим и, строго говоря, также не справедлив для веществ в твердом состоянии. [14]
Закон кратных отношений представляет собой логическое развитие закона постоянства состава. Как выяснилось позже, правы были и Пруст, и Бертолле; последний в своих работах значительно опередил свое время, хотя экспериментальные возможности не позволяли ему строго доказать защищаемые положения. [15]
Страницы: 1 2 3 4