Закон - бойль
Cтраница 3
Закон Бойля - Мариотта устанавливает связь между давлением и объемом данного количества газа при постоянной температуре. [31]
Применяя закон Бойля при решении задач, всегда можно проверить расчеты и определить, приведет ли изменение давления, указанное в задаче, к увеличению или к уменьшению объема, затем можно проверить, согласуется ли полученный ответ с предварительным выводом, сделанным таким образом. [32]
Использовать закон Бойля - Мариотта, в силу которого плотность газа пропорциональна давлению. [33]
Применяя закон Бойля - Мариотта к объему газа, температура которого не меняется, имеем Р PoV0 / Vj 1 05 атм. [34]
Применить закон Бойля - Мариотта. [35]
Графически закон Бойля - Мариотта представлен в системе координат v - р равносторонней гиперболой, показанной на фиг. Как видно из уравнений (2.7) и (2.8) и фиг. Кривая состояний газа, соответствующая данной температуре, всегда расположена тем ближе к осям v и р, чем меньше температура. [36]
Использовать закон Бойля - Мариотта, по которому плотность пропорциональна давлению. [37]
Обобщение законов Бойля - Мариотта и Гей-Люссака дает общее математическое уравнение состояния идеального газа, связы-вающее параметры давления, объема и температуры. [38]
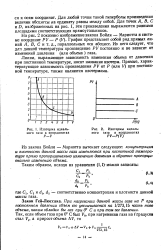 |
Изотерма идеального газа в координатах Р - V.| Изотермы идеального газа в координатах PV - Р ( У. [39] |
Из закона Бойля - Мариотта вытекает следующее: концентрация и плотность данной массы газа изменяются при постоянной температуре прямо пропорционально изменению давления и обратно пропорционально изменению объема. [40]
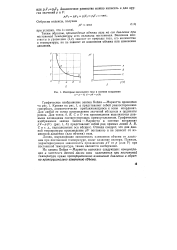 |
Изотермы идеального газа в системе координат. а - р - V. 6 - pV - p ( V. [41] |
Из закона Бойля - Мариотта вытекает следующее: концентрация и плотность данной массы газа изменяются при постоянной температуре прямо пропорционально изменению давления и обрат-но пропорционально изменению объема. [42]
Согласно закону Бойля, при понижении давления газа с 102 до 1 атм объем его должен возрасти в 102 раза. [43]
По закону Бойля - Мариотта р V - p ( V AF) и / 2И2 р ( У 2 - А У) - Складывая эти уравнения, найдем р У1 ртУгр ( у К2), откуда получим для определения рг прежнюю формулу. [44]
По закону Бойля это увеличение давления совершается обратно пропорционально изменению объема. [45]
Страницы: 1 2 3 4