Закон - разбавление
Cтраница 1
 |
Значения., а и К для уксусной кислоты при разных разбавлениях. [1] |
Закон разбавления хорошо применим к слабым электролитам, молекулы которых распадаются на два иона. [2]
Закон разбавления оказался неприменимым к сильным электролитам, так как невозможно было определить их константы диссоциации, Как показали работы позднейших исследователей, понятие о константах диссоциации сильных электролитов совершенно лишено физического смысла. [3]
Закон разбавления принимает тогда вид К. [4]
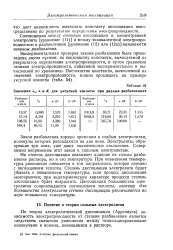 |
Значения 5. к, а и Л для уксусной кислоты при разных разбавлениях. [5] |
Закон разбавления хорошо применим к слабым электролитам, молекулы которых распадаются на два иона. [6]
Закон разбавления принимает тогда вид Ка2С, откуда аУК / С. [7]
Закон разбавления принимает тогда вид Ка. [8]
Законом разбавления часто пользуются для вычисления константы диссоциации слабых электролитов; для этого нужно определить опытным путем степень диссоциации раствора электролита известной концентрации. [9]
Формула закона разбавления является наглядным доказательством высказанного ранее положения о том, что константа электролитической диссоциации характеризует силу электролита. [10]
Если преобразовать закон разбавления, введя понятие разбавление v / n, впервые примененное В. [11]
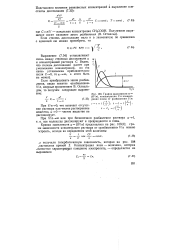 |
График зависимости а f ( V / n, концентрации С и концентрации ионов от разбавления Vim. [12] |
Если преобразовать закон разбавления, введя понятие разбавление VIп, впервые примененное В. [13]
Если преобразовать закон разбавления, введя понятие разбавление V / n, впервые примененное В. [14]
Экспериментальная проверка закона разбавления была произведена двумя путями: по постоянству константы, вычисляемой из результатов определения электропроводности, и путем сравнения величин электропроводности, найденной экспериментально и вычисленной по уравнению. [15]
Страницы: 1 2 3 4