Закон - распределение - молекула
Cтраница 3
Простейшая и практически наиболее важная форма закона распределения молекул по энергиям получается тогда, когда энергия выражена суммой двух квадратичных членов. [31]
Простейшая и практически наиболее важная форма закона распределения молекул по энергиям получается в том случае, если энергию выразить суммой двух квадратичных членов. [32]
 |
Распределение скоростей движения молекул кислорода при 0 С. [33] |
На рисунке 4 в графической форме представлен закон распределения молекул по скоростям. [34]
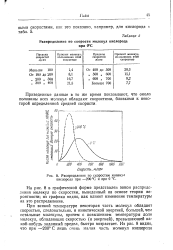 |
Распределение по скоростям молекул кислорода при - 200 С и при О С. [35] |
На рис. 8 в графической форме представлен закон распределения молекул по скоростям, выведенный на основе теории вероятности; из графика видно, как влияет изменение температуры на это распределение. [36]
Соотношение ( 81) известно как уравнение закона распределения молекул по величинам анергии Больцмана. [37]
Соотношение ( 81) известно как уравнение закона распределения молекул по величинам энергии Больцмана. [38]
На основе теории вероятности можно вывести прежде всего закон распределения молекул по скоростям ( закон Максвелла), Этот закон дает возможность определить, какая доля общего числа молекул в данных условиях обладает скоростью, точно отвечающей средней скорости, и какая отличается от нее на ту или другую заданную величину. В математической форме этот закдр выражается сложным соотношением. [39]
В физической химии большое значение имеет установленный Больцманом закон распределения молекул по энергии. Этот закон выражает соотношение между числом молекул данного вида, обладающих различным запасом энергии. [40]
В § 80 второго тома дается термодинамический вывод закона распределения молекул по энергиям Больцмана ( см. следующий параграф), из которого может быть получено распределение по скоростям Максвелла как частный случай. [41]
 |
Молекулы газа могут проходить через отверстие в перегородке сосуда. [42] |
Для вычисления числового значения безразмерного коэффициента С нужно знать закон распределения молекул по направлениям скорости. [43]
Этот закон имеет ту же форму, что и закон распределения молекул газа, но он относится теперь ко всей системе, которая может быть газообразной, жидкой или твердой, и к ее распределению между различными состояниями. Его можно доказать, беря в качестве сложной системы рассматриваемую систему и газ при температуре Т; если эта полная система удовлетворяет микроканонической статистике, то для самой системы отсюда следует каноническое распределение. [44]
Находя максимальное значение энтропии, мы получаем совершенно аналогично классическому случаю закон распределения молекул по энергетическим уровням. [45]
Страницы: 1 2 3 4