Закон - распределение - частица
Cтраница 1
Закон распределения частиц по высоте в равновесном состоянии, аналогичный известной барометрической формуле Лапласа для газов в атмосфере, может быть получен как кинетическим, так и термодинамическим путем. [1]
Обозначив закон распределения частиц на устье, поступивших за время ( L / ( ucp - f04 ( / max)), через. [2]
Нас интересует закон распределения частиц по состояниям. Кроме того, используем статистику Больцмана, согласно которой вероятность нахождения частицы в данном состоянии не зависит от того, имеются ли в данном состоянии другие частицы. [3]
Для нахождения закона распределения частиц по высоте исходят из равенства потоков диффузии и седиментации ( гсед 1диф), т.е. из условия седиментационно - диффузионного равновесия. [4]
Попытки нахождения законов распределения частиц порошков предпринимались многими авторами; были получены формулы, пригодные, однако, только в частных случаях. [5]
Когда полное знание закона распределения частиц не требуется, а достаточно лишь информации о поведении во времени его целых моментов, задача существенно упрощается. Для ядер вида (5.57) - (5.59) она решается точно. [6]
Как и в случае равновесия, знание закона распределения частиц по состояниям позволяет вычислить термодинамические характеристики системы, установить связь между ними, указать закономерности изменения всех величин. К сожалению, реализация этой программы не всегда удается. Трудность состоит в том, что невозможно ввести какие-либо простые функции распределения частиц по состояниям, которые были бы пригодны всегда я везде, как это было для равновесных состояний. В настоящее время разработано много частных подходов, которые были успешно применены для решения отдельных задач. Были выдвинуты и общие методы, которые в принципе пригодны для изучения любой проблемы, однако их использование на практике встречает еще не преодоленные математические затруднения. [7]
Основной задачей статистики коллектива частиц является отыскание закона распределения частиц по скоростям или энергиям. Например, в § § 25.2, 26.10 и 26.11 мы рассмотрели закон распределения газовых молекул по скоростям, установленный Максвеллом, и распределение молекул газа по энергиям р поле силы тяжести. [8]
Одной из основных задач статистической физики является нахождение закона распределения частиц по разным квантовым состояниям. [9]
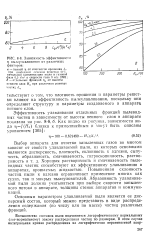 |
Зависимость эффективности т пылеулавливания от различных факторов. [10] |
Большинство составов пыли подчиняется логарифмическому нормальному ( лог-нормальному) закону распределения частиц по размерам. [11]
В работах [2, 3] определены различные физические характеристики маг-нитоожнженных слоев, установлен закон распределения частиц по скоростям, влияние индукции переменного магнитного поля, размера частиц и других параметров на протекающие в слое процессы. Для расчета различных технологических процессов и оптимизации режимных параметров реальных установок необходимо знание характеристик объемных магннто-ожиженных слоев. [12]
Поскольку фундаментальными основами химической термодинамики и кинетики являются закон действующих масс и закон распределения частиц по энергиям, химическая термодинамика и кинетика более близки, чем кинетика и строение вещества или строение вещества и термодинамика. [13]
Поэтому Перрен пошел обходным путем, путем определения средней кинетической энергии w из закона распределения частиц с высотой. [14]
Частицы газа движутся с различными скоростями, им присущи разные температуры, соответствующие закону максвеллов-ского распределения частиц по скоростям. Большинство частиц имеет наиболее вероятную скорость. Однако имеются частицы со скоростями выше и ниже вероятной. Может показаться, что при обычных температурах в газе найдутся частицы с очень высокими скоростями движения ( температурами), которые способны ионизировать нейтральный атом. Однако практически, например при 3000 К, вероятность ионизации газовых частиц исчезающе мала. При более высокой температуре степень термической ионизации становится существенной; в дуговом разряде этот вид ионизации становится преобладающим. [15]
Страницы: 1 2 3